إقحام (كيمياء حيوية)
الإقحام في الكيمياء الحيوية هو إدراج جزيئات بين قواعد الدنا المستوية. تُستخدم هذه العملية كطريقة لدراسة الدنا، كما أنها أساس بعض أنواع التسممات.

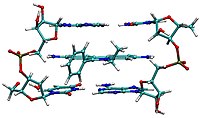
توجد العديد من الجزيئات ( وتعرف كذلك بالربائط) لها القدرة على التآثر مع الدنا. يمكن للربائط التآثر مع الدنا عبر الترابط التساهمي، الترابط الكهروستاتي أو الإقحام.[1] يحدث الإقحام حين تتمكن ربائط بحجمٍ وطبيعةٍ كيميائية مناسبتين من وضع نفسها داخل الفراغ بين أزواج قواعد الدنا، معظم هذه الربائط متعددة الحلقات، عطرية، وذات مستوى واحد، وهي في الغالب أصباغ أحماض نووية جيدة. من المُقْحِمات المدروسة بكثرة: بربارين، بروميد الإيثيديوم، بروفلافين، داونوروبيسين، دوكسوروبيسين وثاليدوميد. تستخدم مقحمات الدنا في العلاج الكيميائي لتثبيط تضاعف الدنا في الخلايا السرطانية المتنامية بسرعة، ومن الأمثلة: دوكسوروبيسين (أدرياميسين) وداونوروبيسين (كلاهما يستخدمان في علاج لمفوما هودجكين)، وداكتينومايسين (يستخدم لعلاج ورم ويلمز، ساركومة يوينغ، الساركومة العضلية المخططة).
المقحمات الفلزية هي مركبات من كايتون فلز ذو ربيطة عطرية متعددة الحلقات، أكثر الأيونات الفلزية استخداما هي الروثينيوم (II)، لأن مركباتها بطيئة جدا في التحلل في الظروف البيولوجية. من بعض الكايتونات الفلزية المستخدمة الأخرى: الروديوم(III) والإريديوم(III). الربائط القياسية المرتبطة بأيون فلزي هي ثنائي البيريدين وثلاثي البيريدين، اللذان لهما بنية مستوية مثالية للإقحام. .[2]
العملية
عدلفي سبيل أن يتمكن المُقحِم من الدخول بين أزواج القواعد، يجب على الدنا فتح فراغٍ بين القواعد وذلك بفك انحنائه. درجة فك الانحناء تختلف بحسب المقحم؛ على سبيل المثال كايتون الإثيديوم (الهيئة الأيونية لبروميد الإيثيديوم الموجودة في محلول مائي) تفك انحناء الدنا بـ26°، في حين أن البروفلافين يفكه بحوالي 17°. يسبب هذا الفك افتراق أزواج القواعد، أو «صعودها» مخلفةً فراغا بحوالي 0.34 نانومتر (3.4 أنغستروم) كما يسبب الفك تغيُّرات بنيوية في سلسلة الدنا: كزيادة طول تلك السلسلة أو طي أزواج القواعد. يمكن أن تؤدي هذه التغيّرات البنيوية إلى تغيّرات وظيفية، في الغالب هي تثبيط عمليات نسخ وتضاعف وترميم الدنا، وهو ما يجعل المقحمات عوامل تطفير قوية. لهذا السبب مقحمات الدنا في الغالب هي عوامل مسرطنة مثل: إكسو (وليس الإندو) 9,8-إيبوكسيد الأفلاتوكسين B1 والأكريدينات مثل بروفلافين أو ميباكرين.
تاريخ
عدلتم اقتراح الإقحام كآلية تآثر بين مركبات كايتونية، مستوية، عطرية ذات أحجام مناسبة (بالنسبة لحجم أزواج القواعد) أول مرة من طرف ليونارد ليرمان سنة 1961.[3][4][5] إحدى الآليات المقترحة هي كالتالي: في محلول مائي متساوي التوتر، ينجذب المقحم الكايتوني إلكتروستاتيا إلى سطح الدنا عديد الأنيون. ثم تقوم الربيطة بإزاحة كايتون الصوديوم و/أو المغنيسيوم الموجودة في «السحابة المكثفة» لهذه الكايتونات المحيطة بالدنا (والتي مهمتها موازنة الشحنات السالبة المحمولة في كل ذرة أكسجين في مجموعة الفوسفات)، وهذا يتسبب في تشكيل ترابط إلكتروستاتي ضعيف مع السطح الخارجي للدنا. من هذه الوضعية تنتشر الربائط على طول سطح الدنا ويمكن أن تتغلغل إلى المحيط الكاره للماء الموجود بين أزواج القواعد الذين قد ينفتح زوج منهم مؤقتا لتشكيل موقع إقحام، وهذا يسمح لللإيثيديوم بالابتعاد عن المحيط المائي الذي يحيط بالدنا إلى موقع الإقحام. تقوم القواعد بشكيل موقع إقحام مؤقتا بسبب الطاقة الممتصة اثناء الاصطدام بجزيئات المذيب.
انظر أيضا
عدلمراجع
عدل- ^ Richards, A. D.؛ Rodgers, A. (2007). "Synthetic metallomolecules as agents for the control of DNA structure". Chemical Society Reviews. ج. 36 ع. 3: 471–83. DOI:10.1039/b609495c. PMID:17325786.
- ^ Schatzschneider، Ulrich (2018). "Chapter 14. Metallointercalators and Metalloinsertors: Structural Requirements for DNA Recognition and Anticancer Activity". في Sigel، Astrid؛ Sigel، Helmut؛ Freisinger، Eva؛ Sigel، Roland K. O. (المحررون). Metallo-Drugs: Development and Action of Anticancer Agents. Berlin: de Gruyter GmbH. ج. 18. ص. 387–435. DOI:10.1515/9783110470734-020.
- ^ Lerman, L. S. (1961). "Structural considerations in the interaction of DNA and acridines" (PDF). Journal of Molecular Biology. ج. 3 ع. 1: 18–30. DOI:10.1016/S0022-2836(61)80004-1. PMID:13761054. مؤرشف من الأصل (PDF) في 2016-10-20.
- ^ Luzzati, V.؛ Masson, F.؛ Lerman, L. S. (1961). "Interaction of DNA and proflavine: A small-angle x-ray scattering study". Journal of Molecular Biology. ج. 3 ع. 5: 634–9. DOI:10.1016/S0022-2836(61)80026-0. PMID:14467543.
- ^ Lerman, L. S. (1963). "The structure of the DNA-acridine complex". Proceedings of the National Academy of Sciences of the United States of America. ج. 49 ع. 1: 94–102. DOI:10.1073/pnas.49.1.94. PMC:300634. PMID:13929834.