جابابنتينويد
جابابنتينويد (بالإنجليزية: Gabapentinoids) (اسم العلامة التجارية جابابنتينويد) يُعرف أيضًا بربيطة ألفا 2 دلتا، صنف دوائي مشتق من حمض الغاما أمينو-بيوتيريك المثبط (غابا) (أي نظائر غابا) التي تحصر الوحدات الفرعية من ألفا 2 دلتا الحاوية على قنوات كالسيوم معتمدة على الفولتاج. يُشار إلى هذا الموقع باسم مستقبل غابابنتين (وحدة ألفا 2 دلتا الفرعية)، ويُعد هدفًا لدوائي غابابنتين وبريغابالين.[1][2]
| جابابنتينويد | |
|---|---|
| صنف دوائي | |
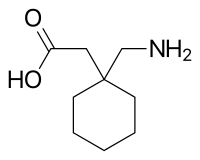 جابابنتينويد | |
| معرفات الصنيف | |
| المرادفات | α2δ ligands; Ca2+ α2δ ligands |
| الاستعمال | صرع، ألم عضلي ليفي، ألم عصبي تال للهربس |
| رمز ATC | N03AX |
| المستهدف الحيوي | α2δ subunit-containing VDCCs |
| في ويكي بيانات | |
تشمل مركبات الجابابنتينويد المستخدمة سريريًا كلًا من: غابابنتين، بريغابالين، ميروغابالين، وطليعة دواء غابابنتين المسمى غابابنتين إيناكاربيل.[2][3]
يؤدي مركب فنيبوت أيضًا دور الجابابنتينويدات ذاته إضافةً على كونه ناهضًا لمستقبلات جابا ب. ما تزال النظائر الأخرى مثل إيماغابالين في مرحلة التجارب السريرية ولم يوافق على استخدامها بعد. تشمل الأدوية الأخرى المستخدمة في الأبحاث العلمية دون أن تحظى بالموافقة الطبية «أتاغابالين» و «4-ميتيل بريغابالين» و«بّي دي 217,014».[4][5]
الاستخدامات السريرية
عدلحظيت مركبات جابابنتينويد بموافقة الاستخدام لعلاج كل من الصرع والألم العصبي التالي للهربس وألم الاعتلال العصبي واعتلال الأعصاب السكري والألم العضلي الليفي واضطراب القلق العام ومتلازمة تململ الساقين. هناك بعض الاستخدامات غير المصرح بها مثل الأرق والصداع النصفي (الشقيقة) واضطراب القلق الاجتماعي والهلع والهوس واضطراب ثنائي القطب ومتلازمة الانسحاب الكحولي. ما زالت الأدلة محدودةً على فعالية الدواء في علاج الألم الحاد أسفل الظهر، إذ يرتفع خطر حدوث الآثار الجانبية دون فوائد تُذكر. تشمل الآثار الجانبية الرئيسة: الشعور بالنعاس والتعب، وانخفاض ضغط الدم، والغثيان والإقياء، والهلاوس البصرية الزرقية التي تظهر نموذجيًا عند استخدام المهلوسات.[6][7]
علم الأدوية
عدلالديناميكية الدوائية
عدلتمثل مركبات الجابابنتينويد مجموعةً من الربائط في مواقع الوحدات الفرعية ألفا 2 دلتا الإضافية الخاصة بقنوات الكالسيوم المعتمدة على الفولتاج، وبالتالي تثبط الوحدات الفرعية الحاملة لهذه القنوات. هناك وحدتان فرعيتان رابطتان للدواء: ألفا 2 دلتا-1 وألفا 2 دلتا-2، وتبدي مركبات الجابابنتينويد ألفةً متشابهةً لهذين الموقعين (وبالتالي لا تمتاز بالانتقائية بينهما، لكنها تُعد انتقائيةً للوحدة الفرعية الحاملة لقنوات الكالسيوم المعتمدة على الفولتاج). يرتبط دواء فنيبوت بمستقبلات جابا بي بألفة أضعف (خمسة إلى عشرة أضعاف في أحد الدراسات) ويؤدي دور ناهض دوائي، وتُعد هذه ميزةً فريدةً له.[8][9]
رغم كون مركبات جابابنتينويد نظائر جابا، لا يرتبط الغابابنتين والبريغابالين مع مستقبلات جابا، ولا يتحولان إلى مركبات جابا أو ناهضات مستقبلاته في الكائن الحي، ولا يعدلان نقله أو استقلابه. لا يوجد حاليًا أي دليل على أن تأثيرات الغابابنتين والبريغابالين تتواسط عبر أي آلية عدا تثبيط وحدات ألفا 2 دلتا الفرعية الحاوية على قنوات الكالسيوم الشاردية المعتمدة على الفولتاج. وُجد أن مركبات الجابابنتينويد مثل الغابابنتين تنشط قنوات البوتاسيوم المعتمدة على الفولتاج، وهذا لا ينطبق على البريغابالين.[10]
يُعد الحمضان الأمينيان ل-ليوسين ول-إيزوليوسين داخليا المنشأ ربيطتين بارزتين للوحدات الفرعية ألفا 2 دلتا الحاملة لقنوات الكالسيوم الشاردية المعتمدة على الفولتاج، إذ تشابه بنيتهما الكيميائية مركبات الجابابنتينويد إلى حد كبير، مع ألفة مشابهة للغابابنتين والبريغابالين (تركيز المادة الموافق للتثبيط النصفي = 71 نانومولار بالنسبة لحمض ل-إيزوليوسين)، وتوجد في السائل الدماغي الشوكي عند البشر بتراكيز ميكرومولارية (ل-ليوسين: 12.9 ميكرومولار، ل-إيزوليوسي: 4.8 ميكرومولار).
اقترحت إحدى الفرضيات أن هذين الحمضين قد يمثلان ربائط داخلية المنشأ للوحدات الفرعية وقد يثبطان تنافسيًا تأثيرات الجابابنتينويد. يملك الغابابنتين والبريغابالين ألفةً نانومولارية للوحدات الفرعية ألفا 2 دلتا، لكن تظهر فعاليتهما لدى الأحياء عند تراكيز ميكرومولارية منخفضة، ويعتقد أن التنافس على الارتباط مع الحمضين الأمينيين السابقين يمثل الآلية المسؤولة عن هذا التفاوت بين الوسطين المخبري والحي.[11]
في إحدى الدراسات، وُجد أن قيم الألفة التي أبدتها مركبات الجابابنتينويد لوحدات ألفا 2 دلتا المعبر عنها في أدمغة الجرذان بلغت 0.05 ميكرومولارًا للغابابنتين و23 ميكرومولارًا للفنيبوت-(آر) و39 ميكرومولارًا للفنيبوت-(إس) و156 ميكرومولارًا للباكلوفين. بلغت ألفة هذه الأدوية لمستقبلات جابا بي <1 ميليمولارًا للغابابنتين و92 ميكرومولارًا للفنيبوت-(آر) و<1 ميليمولارًا للفنيبوت-(إس) و6 ميكرومولارًا للباكلوفين. لا تُعد ألفة الباكلوفين لمستقبلات ألفا 2 دلتا ذات أهمية سريرية بسبب انخفاضها مقارنةً بألفته لمستقبلات جابا بي (26 ضعفًا). أبدى البريغابالين فعاليةً أكبر (نحو مرتين ونصف) من الغابابنتين في الدراسات السريرية.[12]
الحرائك الدوائية
عدلالامتصاص
عدليُمتص الغابابنتين والبريغابالين من الأمعاء عبر آلية النقل النشط المتواسط بناقل الحموض الأمينية المحايدة الكبير (LAT1, SLC7A5)، وهو ناقل للحموض الأمينية مثل ل-ليوسين ول-فينيل ألانين. لا يعمل هذا الناقل سوى على عدد محدود جدًا من الأدوية (أقل من عشرة). يبدو أن بريغابالين يُنقل عبر حوامل أخرى أيضًا على عكس الغابابنتين الذي يُنقل عبر مركبات أخرى. يصل هذا الناقل إلى مرحلة الإشباع بسهولة، لذا تعتمد الحرائك الدوائية للغابابنتين على الجرعة، فينقص توافره الحيوي ويتأخر وصوله إلى ذروة تركيزه في الجرعات المرتفعة. لا يحدث هذا مع البريغابالين الذي يُظهر حرائك دوائيةً خطيةً دون إشباع الامتصاص. يُنقل غابابنتين إيناكاربيل بأسلوب مشابه عبر ناقل أحادي الكاربوكسيلات 1 (إم سي تي 1) وناقل عديد الفيتامينات المعتمد على الصوديوم وليس عبر LAT1، ولا يحدث إشباع في التوافر الحيوي حتى بلوغ جرعة 2,800 مغ. يسلك الباكلوفين سلوكًا مشابهًا للغابابنتين والبريغابالين، إذ يمثل نظيرًا للفنيبوت (بالتحديد 4-كلوروفنيبوت) وينقل عبر LAT1، لكنه ركيزة ضعيفة لهذا الناقل.[13]
يبلغ التوافر الحيوي الفموي للغابابنتين 80% تقريبًا عند جرعة 100 مغ ثلاث مرات يوميًا كل ثماني ساعات، لكنه ينقص إلى 60% عند جرعة 300 مغ، و47% عند جرعة 400 مغ، و34% عند جرعة 800 مغ، و27% مغ عند جرعة 1,600 مغ إذ أعطيت جميعًا وفق ذات الخطة العلاجية. على النقيض، يُعد التوافر الحيوي للدواء الفموي أعلى من 90% أو مساويًا لهذه النسبة تقريبًا مهما كانت الجرعة العلاجية ضمن المجال 75 إلى 900 مغ/يوم. لا يؤثر الطعام كثيرًا على التوافر الحيوي للبريغابالين، لكن بالمقابل، يزيد الطعام من المستويات في المنطقة تحت المنحنى للغابابنتين بنحو 10%. يمكن أن تزيد الأدوية التي تطيل زمن نقل الغابابنتين في المعي الدقيق من توافره الحيوي الفموي. يزيد التوافر الحيوي للدواء بنسبة 50% عند إعطائه بجرعة 600 مغ بالاشتراك مع المورفين الفموي (الذي يبطئ التمعجات المعوية).[14]
يزيد التوافر الحيوي لبريغابالين إيناكاربيل (كما هو الحال في الغابابنتين) عن 68% أو يساويها عند جميع الجرعات المعطاة (حتى 2,800 مغ)، ويبلغ وسطيًا 75%. على نقيض مركبات الجابابنتينويد الأخرى، لم تُدرس الحرائك الدوائية للفنيبوت بما يكفي، وما يزال توافره الحيوي الفموي مجهولًا، لكن يبدو أنه يبلغ 63% على الأقل عند إعطاء جرعة مفردة بمقدار 250 مغ بناءً على عدم تغير القسم المقاس منه في البول لدى المتطوعين الأصحاء المتناولين لهذه الجرعة.[15]
يملك غابابنتين في الجرعات المنخفضة حتى 100 مغ زمن تركيز أعظمي (الزمن اللازم للوصول إلى ذروة التركيز) يقارب 1.7 ساعة، بينما يزيد هذا الزمن إلى 3 أو 4 ساعات في الجرعات الأعلى. يبلغ زمن التركز الأعظمي للبريغابالين ساعةً أو أقل عمومًا عند جرعة 300 مغ أو أقل، لكن وُجد أن تناول الطعام يؤخر كثيرًا من امتصاصه وينقص بشدة من مستويات الذروة دون التأثير على توافره الحيوي. تبلغ قيم زمن التركيز الأعظمي للبريغابالين 0.6 ساعة في حالة الصيام و3.2 ساعة عند تناول الطعام (فارق بمقدار خمسة أضعاف)، بينما ينقص التركيز الأعظمي بنسبة 25-31% عند تناول الطعام مقارنةً بوضعية الصيام.[16]
على عكس البريغابالين، لا يؤثر الطعام كثيرًا على زمن التركيز الأعظمي للغابابنتين، ويزيد تركيزه المصلي الأعظمي بما يقارب 10%. تبلغ قيمة زمن التركيز الأعظمي للشكل سريع التحرر من غابابنتين إيناكاربيل (مثل الغابابنتين النشط) نحو 2.1 إلى 2.6 ساعات مهما كانت جرعته العلاجية (بين 350 و 2,800 مغ) في نظام الجرعة الوحيدة، بينما تبلغ قيمته 1.6 - 1.9 ساعات على مدى جرعته العلاجية (350-2,100 مغ) عند اعتماد نظام الجرعات المتكررة.
يبلغ زمن التركيز المصلي الأعظمي في الشكل مديد التحرر من غابابنتين إيناكاربيل نحو 5.1 ساعة عند تناول جرعة مفردة تبلغ 1,200 مغ في حالة الصيام، و8.4 ساعات عند تناول جرعة مفردة تبلغ 1,200 مغ في حالة الإطعام. لم يُدرس بعد زمن التركيز الأعظمي للفنيبوت، لكن بدء الفعالية وتأثيرات الذروة تحدث خلال 2 إلى 4 ساعات و5 إلى 6 ساعات على الترتيب بعد الابتلاع الفموي لجرعات عالية (1-3 غ) لدى متعاطي المخدرات الترفيهية.
المراجع
عدل- ^ Eroglu، Çagla؛ Allen، Nicola J.؛ Susman، Michael W.؛ O'Rourke، Nancy A.؛ Park، Chan Young؛ Özkan، Engin؛ Chakraborty، Chandrani؛ Mulinyawe، Sara B.؛ Annis، Douglas S.؛ Huberman، Andrew D.؛ Green، Eric M.؛ Lawler، Jack؛ Dolmetsch، Ricardo؛ Garcia، K. Christopher؛ Smith، Stephen J.؛ Luo، Z. David؛ Rosenthal، Arnon؛ Mosher، Deane F.؛ Barres، Ben A. (2009). "Gabapentin Receptor α2δ-1 is a Neuronal Thrombospondin Receptor Responsible for Excitatory CNS Synaptogenesis". Cell. ج. 139 ع. 2: 380–92. DOI:10.1016/j.cell.2009.09.025. PMC:2791798. PMID:19818485.
- ^ ا ب Honorio Benzon؛ James P. Rathmell؛ Christopher L. Wu؛ Dennis C. Turk؛ Charles E. Argoff؛ Robert W Hurley (11 سبتمبر 2013). Practical Management of Pain. Elsevier Health Sciences. ص. 1006. ISBN:978-0-323-17080-2. مؤرشف من الأصل في 2021-10-24.
- ^ Elaine Wyllie؛ Gregory D. Cascino؛ Barry E. Gidal؛ Howard P. Goodkin (17 فبراير 2012). Wyllie's Treatment of Epilepsy: Principles and Practice. Lippincott Williams & Wilkins. ص. 423. ISBN:978-1-4511-5348-4. مؤرشف من الأصل في 2021-11-11.
- ^ Vinik، Aaron؛ Rosenstock، Julio؛ Sharma، Uma؛ Feins، Karen؛ Hsu، Ching؛ Merante، Domenico (2014). "Efficacy and Safety of Mirogabalin (DS-5565) for the Treatment of Diabetic Peripheral Neuropathic Pain: A Randomized, Double-Blind, Placebo- and Active Comparator–Controlled, Adaptive Proof-of-Concept Phase 2 Study". Diabetes Care. ج. 37 ع. 12: 3253–61. DOI:10.2337/dc14-1044. PMID:25231896.
- ^ Zvejniece L، Vavers E، Svalbe B، Veinberg G، Rizhanova K، Liepins V، Kalvinsh I، Dambrova M (2015). "R-phenibut binds to the α2-δ subunit of voltage-dependent calcium channels and exerts gabapentin-like anti-nociceptive effects". Pharmacol. Biochem. Behav. ج. 137: 23–9. DOI:10.1016/j.pbb.2015.07.014. PMID:26234470. S2CID:42606053.
- ^ "Buy Advil and Ibuprofen Tablets Online - HealthWarehouse - HealthWarehouse.com". HealthWarehouse (بالإنجليزية). Archived from the original on 2021-08-10. Retrieved 2021-08-13.
- ^ Shanthanna، Harsha؛ Gilron، Ian؛ Rajarathinam، Manikandan؛ AlAmri، Rizq؛ Kamath، Sriganesh؛ Thabane، Lehana؛ Devereaux، Philip J.؛ Bhandari، Mohit؛ Tsai، Alexander C. (15 أغسطس 2017). "Benefits and safety of gabapentinoids in chronic low back pain: A systematic review and meta-analysis of randomized controlled trials". PLOS Medicine. ج. 14 ع. 8: e1002369. DOI:10.1371/journal.pmed.1002369. PMC:5557428. PMID:28809936.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Sills GJ (2006). "The mechanisms of action of gabapentin and pregabalin". Curr Opin Pharmacol. ج. 6 ع. 1: 108–13. DOI:10.1016/j.coph.2005.11.003. PMID:16376147.
- ^ Uchitel OD، Di Guilmi MN، Urbano FJ، Gonzalez-Inchauspe C (2010). "Acute modulation of calcium currents and synaptic transmission by gabapentinoids". Channels (Austin). ج. 4 ع. 6: 490–6. DOI:10.4161/chan.4.6.12864. PMID:21150315.
- ^ Stahl SM، Porreca F، Taylor CP، Cheung R، Thorpe AJ، Clair A (2013). "The diverse therapeutic actions of pregabalin: is a single mechanism responsible for several pharmacological activities?". Trends Pharmacol. Sci. ج. 34 ع. 6: 332–9. DOI:10.1016/j.tips.2013.04.001. PMID:23642658.
- ^ Davies A، Hendrich J، Van Minh AT، Wratten J، Douglas L، Dolphin AC (2007). "Functional biology of the alpha(2)delta subunits of voltage-gated calcium channels". Trends Pharmacol. Sci. ج. 28 ع. 5: 220–8. DOI:10.1016/j.tips.2007.03.005. PMID:17403543.
- ^ Schifano F، D'Offizi S، Piccione M، Corazza O، Deluca P، Davey Z، Di Melchiorre G، Di Furia L، Farré M، Flesland L، Mannonen M، Majava A، Pagani S، Peltoniemi T، Siemann H، Skutle A، Torrens M، Pezzolesi C، van der Kreeft P، Scherbaum N (2011). "Is there a recreational misuse potential for pregabalin? Analysis of anecdotal online reports in comparison with related gabapentin and clonazepam data". Psychother Psychosom. ج. 80 ع. 2: 118–22. DOI:10.1159/000321079. hdl:2299/9328. PMID:21212719. S2CID:11172830.
- ^ Dickens D، Webb SD، Antonyuk S، Giannoudis A، Owen A، Rädisch S، Hasnain SS، Pirmohamed M (2013). "Transport of gabapentin by LAT1 (SLC7A5)". Biochem. Pharmacol. ج. 85 ع. 11: 1672–83. DOI:10.1016/j.bcp.2013.03.022. PMID:23567998.
- ^ Kido Y، Tamai I، Uchino H، Suzuki F، Sai Y، Tsuji A (2001). "Molecular and functional identification of large neutral amino acid transporters LAT1 and LAT2 and their pharmacological relevance at the blood-brain barrier". J. Pharm. Pharmacol. ج. 53 ع. 4: 497–503. DOI:10.1211/0022357011775794. PMID:11341366. S2CID:38717319.
- ^ Bockbrader HN، Wesche D، Miller R، Chapel S، Janiczek N، Burger P (2010). "A comparison of the pharmacokinetics and pharmacodynamics of pregabalin and gabapentin". Clin Pharmacokinet. ج. 49 ع. 10: 661–9. DOI:10.2165/11536200-000000000-00000. PMID:20818832. S2CID:16398062.
- ^ Lapin، I. (2001). "Phenibut (beta-phenyl-GABA): A tranquilizer and nootropic drug". CNS Drug Reviews. ج. 7 ع. 4: 471–481. DOI:10.1111/j.1527-3458.2001.tb00211.x. PMC:6494145. PMID:11830761.