نسخ أولي
النسخ الأولي أو رنا المرسال الأولي هو منتج الحمض الريبي النووي المنفرد والذي تم تصنيعه عن طريق نسخ الحمض النووي (DNA)، ومعالجته لانتاج الحمض النووي الريبي الجاهز للاستخدام في جميع انواعه مثل النسخ الأولي للرنا الرسول (mRNA)، الحمض النووي الريبي الناقل (tRNA)، الحمض النووي الريبي الرايبوزوم (rRNA). ان عمليه النسخ الأولي تعمل على تعديل الحمض النووي الريبي الرسول (mRNA) وتجهيزه لعمليه الترجمة. على سبيل المثال، النسخ الأولي للرنا الرسول (Pre-mRNA) يعتبر جزء من عمليه النسخ الأولي الذي ينتج منها mRNA بعد معالجة الحمض النووي الريبوزي.

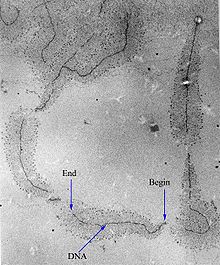
يتم تكوين النسخ الأولي Pre-mRNA من الحمض النووي (DNA) في نواة الخلية عن طريق النسخ. النسخ الأولي للرنا الرسول Pre-mRNA يضم الجزء الأكبر من الحمض النووي الريبي النووي غير المتجانس (hnRNA). وبمجرد ما تنتهي عمليه النسخ الأولي Pre-mRNA ينتج الحمض النووي الرسول(mRNA). غالبًا ما يستخدم مصطلح الحمض النووي الريبي النووي غير المتجانس (hnRNA) كمرادف للنسخ الأولي (Pre-mRNA)، على الرغم من أن الحمض النووي الريبي النووي غير المتجانس (hnRNA) قد يتضمن نسخًا من الرنا الذي لا ينتهي في النهاية إلى الحمض النووي الريبي الرسول (mRNA) السيتوبلازمي.
هناك العديد من الخطوات التي تساهم في إنتاج النسخ الاولي. تشمل كل هذه الخطوات سلسلة من التفاعلات لبدء واستكمال نسخ الحمض النووي (DNA) في نواة حقيقيات النوى.تقوم بعض العوامل أدوارًا رئيسية في تنشيط وتثبيط النسخ، حيث تنظم إنتاج النسخ الأساسي. ينتج النسخ النسخ الاولي التي يتم تعديلها بشكل أكبر من خلال العديد من العمليات. وتشمل هذه العمليات الحد الأقصى cap 5 ' ، 3'-polyadenylation ، والربط البديل. ان الربط البديل يساهم بشكل مباشر في تنوع الحمض النووي الريبي الرسول (mRNA) الموجود في الخلايا. تمت دراسة تعديلات النصوص الأولية في الأبحاث التي تسعى إلى معرفة أكبر لدور هذه النسخ وأهميتها. تعتمد الدراسات التجريبية على التغييرات الجزيئية في عمليه النسخ الأولية والعمليات قبل وبعد النسخ إلى فهم أكبر للأمراض التي تندرج تحت عمليه النسخ الأولية.
إنتاج
عدلالخطوات التي تساهم في إنتاج النسخ الأولية تشمل على سلسلة من التفاعلات الجزيئية التي تبدأ بنسخ الحمض النووي DNA داخل نواة الخلية. اعتمادا على احتياجات خلية معروفه، سلسلات معينه من الحمض النووي يتم نسخها لإنتاج مجموعة متنوعة من منتجات الحمض النووي الريبي لترجمتها إلى بروتينات وظيفية للاستخدام الخلوي. لبدء عملية النسخ في نواة الخلية، حلقات الحمض المزدوج غير قابلة للكسر وروابط الهيدروجين التي تربط الأحماض النووية الملائمه مع الحمض النووي تكسر لإنتاج حلقتين أحادي الحمض النووي أحادي الوصل.[1] حلقه واحدًا من قالب الحمض النووي تستخدم من أجل نسخ نسخه اوليه من الحمض النووي الريبي الرسول mRNA .الحمض النووي هذا يرتبط عن طريق بوليميريز الحمض النووي الريبي في منطقة محفز promoter للحمض النووي.[2]
في حقيقيات النوى، ثلاثة أنواع من الحمض النووي الريبي RNA- الحمض النووي الريبي الرايبوسوم (rRNA) ، الحمض النووي الريبي الناقل(tRNA) ، والحمض النووي الريبي الرسول mRNA، يتم انتاجها من بوليمرات الحمض النووي الريبي الرنا بينما في بدائيات النوى فيوجد بوليمر واحد (سلسلة واحدة) الرنا لانتاج كل الأنواع الأخرى للرنا.[3] بوليميريز الحمض النووي الريبي (II) من حقيقيات النوى ينسخ إلى نسخة أولية، وهي نسخة مخصصة للمعالجة في الحمض النووي الريبي الرسول mRNA ، من قالب الحمض النووي المضاد للحساسية في اتجاه 5«إلى 3»، وهذا النص الأساسي المركب حديثًا مكمل لجزء مضاد الحمض النووي للحمض النووي.[1] يبني RNA polymerase II النسخة الأولية باستخدام مجموعة من أربعة مخلفات أحادية الفوسفات ريبونوكلوسيد محددة (أحادي فوسفات الأدينوساين (AMP)، أحادي فوسفات سيتيني (CMP)، أحادي فوسفات غوانوزين (GMP)، يوريدين أحادي الفوسفات (UMP) 3 'مجموعة الهيدروكسيل في نهاية 3' من mRNA المتنامية.[1]
تكشف الدراسات عن النسخ الأولية التي ينتجها RNA polymerase II أن متوسط النسخة الأولية يبلغ 7000 نيوكليوتيد في الطول، وبعضها ينمو بطول 20.000 نيوكليوتيد.[2] إن تضمين تسلسل إكسون وإنترون ضمن النصوص الأولية يفسر الفرق في الحجم بين النصوص الأولية الأكبر ومرنا الأصغر حجماً الناضجة الجاهزة للترجمة إلى بروتين.
التنظيم
عدليساهم عدد من العوامل في تنشيط وتثبيط النسخ وبالتالي تنظيم إنتاج النسخ الأولية من حمض نووي (DNA) معين.
غالبًا ما يتم التحكم في تنشيط نشاط بوليميريز الحمض النووي الريبي (RNA) لإنتاج النسخ الأولي عن طريق سلاسل الحمض النووي (DNA) المعزز. عوامل النسخ، البروتينات التي ترتبط بعناصر الحمض النووي لتنشيط أو تثبيط عمليه النسخ، ترتبط معززات وتوظيف إنزيمات تغيّر مكونات النوكليوزوم، ويتسبب في أن يكون الحمض النووي (DNA) متاحًا بشكل أو بآخر للوصول إلى بوليميريز الحمض النووي الريبي (RNA). تحدد المركبات الفريدة اما تنشيط أو تثبيط عوامل النسخ التي ترتبط بمناطق الحمض النووي (DNA) المحسن تحدد إذا كان الجين المحسن الذي يتفاعل معه قد تم تنشيطه أم لا.[4] يعتمد تنشيط النسخ على ما إذا كانت عمليه النسخ مطوله ومعقده أم لا، الذي يتكون من مجموعة من عوامل النسخ، يمكن أن يحفز بوليميريز الحمض النووي الريبي (RNA) على الانفصال عن الوسط المعقد الذي يربط منطقة التعزيز مع (promoter).[4]
تثبيط نشاط بوليميريزالحمض النووي الريبي (RNA) يمكن تنظيمه من خلال تسلسل الحمض النووي (DNA) الذي يسمى كواتم الصوت. مثل المحسّنات، قد توجد كواتم الصوت في مواقع أبعد أو أسفل المورثات من الجينات التي تنظمها. ترتبط تسلسلات الحمض النووي (DNA) هذه بالعوامل التي تساهم في اضطراب استقرار مجمع البدء اللازم لتنشيط بوليميريز الحمض النووي الريبي، وبالتالي تمنع النسخ.[5]
يتم تعديل هيستون بواسطة عوامل النسخ التي يعد عوامل تنظيميه رئيسيه أخرى للنسخ بواسطة بوليميريزالحمض النووي الريبي RNA. بشكل عام، والعوامل التي تؤدي إلى هيستون acetylation تفعل النسخ بينما العوامل التي تؤدي إلى هيستون deacetylation تمنع النسخ.[6] أسيتيل هيستونينتج عن التنافر بين المكونات السلبية داخل النيوكليوزومات، مما يسمح للوصول إلى بوليميريز الحمض النووي الريبي (RNA).
Deacetylation للهستونات المستقره الملفوفة بإحكام حول النوكليوزومات، يمنع الوصول إلى بوليميريزالحمض النووي الريبي RNA. بالإضافة إلى أنماط acetylation من هيستون، انماط methylation في مناطق promoter للحمض النووي (DNA) تنظم وصول بوليميريزالحمض النووي الريبي (RNA)إلى قالب معين. غالبًا ما يكون بوليميريز الحمض النووي الريبي (RNA)غير قادرعلى إنتاج نسخة أولية إذا كانت منطقة الجينات المستهدفة (promoter) تحتوي على السيتوزينات المحددة الميثيلية - البقايا التي تمنع ارتباط عوامل تنشيط النسخ وتوظيف إنزيمات أخرى لتثبيت بنية النيكلوزوم المرتبطة بإحكام، مع استبعاد الوصول إلى بوليميريز الحمض النووي الريبي (RNA) ومنع إنتاج عمليه النسخ الاولي.[4]
R-الحلقات
عدلتتشكل حلقات R أثناء النسخ. حلقة R - هي بنية حمض نووي ثلاثية تحتوي على منطقة مهجنه من الحمض النووي الريبي (RNA) والحمض النووي (DNA) المفرد غير المرتبط به. غالبًا ما تشكل مناطق النسخ النشطه من الحمض النووي (DNA)حلقات R غير المحميه التي تؤدي إلى تلف الحمض النووي. تقلل الإنترونات من تشكل حلقة R وتلف الحمض النووي في جينات الخميرة عالية التعبير.[7]
معالجة الحمض النووي الريبي
عدلالنسخ، وهي مرحلة منظمة بشكل كبير في التعبير الجيني، وتنتج النسخ الأولية. لكن، النسخة هي فقط الخطوة الأولى التي يجب أن يتبعها العديد من التعديلات التي تنتج عن أشكال وظيفية من الحمض النووي الريبي (RNAs). على خلاف ذلك، النسخ الأولية المركّبة حديثًا يتم تعديلها بعدة طرق لتحويلها إلى أشكالها الوظيفية الناضجة لإنتاج بروتينات احماض امينيه ريبيه مختلفة مثل mRNA , tRNA و rRNA .
معالجة
عدلعملية تعديل النسخة الأساسية الأولية متشابه للـ tRNA والـ rRNA في كل من الخلايا حقيقية النواة وبدائيه النواة. من ناحية أخرى، معالجة النسخ الأولية تختلف في mRNAs للخلايا بدائية النواة والخلايا حقيقية النواة.[8] على سبيل المثال، تعمل بعض mRNAs البكتيرية بدائية النواة كقوالب لتكوين البروتينات في نفس الوقت الذي يتم فيه إنتاجها عن طريق النسخ. بدلاً من هذا، ما قبل الحمض النووي الريبي الرسول للخلايا حقيقية النواة يمر بمجموعة واسعة من التعديلات قبل نقلها من النواة إلى السيتوبلازم حيث يتم ترجمة أشكالها الناضجة.[8] هذه التعديلات مسؤولة عن أنواع مختلفة من الرسائل المشفرة التي تؤدي إلى ترجمة أنواع مختلفة من المنتجات. أيضا، عمليه النسخ الاوليه توفرتحكم على التعبير الجيني وكذلك آلية تنظيمية لمعدلات تحلل الحمض النووي الريبي الرسول. تشتمل معالجة ما قبل الحمض النووي الريبي الرسول في الخلايا حقيقية النواة على 5 أغطية و3Polyadenylation والتشكيل البديل (alternative splicing).
5 'متوجا
عدلبعد وقت قصير من بدء النسخ في حقيقيات النوى، يتم تعديل نهاية ما قبل الحمض النووي الريبي الرسول 5 '(Pre-mRNA) عن طريق اضافه من غطاء 7-methylguanosine ، المعروف أيضًا باسم الحد 5 '.[8] يبدأ تعديل الحد الأقصى 5 عن طريق إضافة GTP إلى النوكليوتيدات الطرفية 5 'من مرحلة ما قبل الحمض النووي الريبي الرسول (Pre-mRNA) في الاتجاه المعاكس مع إضافة مجموعات الميثيل إلى بقايا G.[8] غطاء 5' ضروريًا لإنتاج الحمض النووي الريبي الرسول (mRNA) الوظيفي لأن الغطاء 5' هو المسؤول عن محاذاة الحمض النووي الريبي الرسول (mRNA) مع الريبوسوم أثناء الترجمة.[8]
تذييل بعديد الأدينيلات
عدلفي حقيقيات النوى، يعدل الأدينيل الإيثيليول أكثر من mRNAs والتي يتم خلالها إضافة بنية تسمى ذيل poly-A .[8] يتم الكشف عن إشارات polyadenylation ، والتي تشمل العديد من عناصر تسلسل الحمض النووي الريبي، من قبل مجموعة من البروتينات التي تشير إلى إضافة ذيل poly-A (حوالي 200 نيوكليوتيدات في الطول). يوفر تفاعل polyadenylation إشارة لنهاية النسخ وهذا التفاعل ينتهي بحوالي بضع مئات من النيوكليوتيدات في اتجاه مجرى النهر من موقع الذيل poly-A.[8]
الربط البديل
عدلما قبل الحمض النووي الريبي الرسول (mRNA)في كائنات حقيقيات النواة لها الإنترونات التي تقسمها spliceosomesالمتكونة من البروتينات النووية الصغيرة (small nuclear ribonucleoproteins).[9][10]
في الخلايا حقيقية النواة المعقدة، نحتاج إلى عمليه نسخ اولي واحده لتحضير كميات كبيرة من الحمض النووي الريبي الرسول (mRNA) الناضج بسبب عمليه الربط البديل. يتم تنظيم عمليه الربط البديل بحيث يمكن لكل حمض نووي ريبي رسول (mRNA) ناضج تشفير العديد من البروتينات.
يمكن ملاحظة تأثير الربط البديل في التعبير الجيني في حقيقيات النوى المعقدة التي تحتوي على عدد ثابت من الجينات في جينومها ولكنها تنتج أعدادًا أكبر بكثير من منتجات الجينات المختلفة.[8] في معظم حقيقيات النوى ما قبل الحمض النووي الريبي الرسول (mRNA) تحتوي على العديد من الإنترونات والإكسونات. ان التركيبات المختلفة المحتملة لمواقع 5 و 3 في ما قبل الحمض النووي الريبي الرسول (mRNA) تؤدي إلى أخذ مجموعة من الإكسونات بينما يتم التخلص من الإنترونات من الحمض النووي الريبي الرسول (mRNA) الناضج. وبالتالي، يتم إنشاء أنواع مختلفة من الحمض النووي الريبي الرسول (mRNA) الناضج.[8] يحدث الربط البديل في البروتينات الكبيره المعقده تسمى ب spliceosome . الربط البديل أمرمهم للأنسجة المحدده وتطوير عمليه التنظيم في التعبير الجيني.[8] يمكن أن يتأثر الربط البديل بعوامل مختلفة، بما في ذلك الطفرات مثل تغير موقع الكروموسومات.
في بدائيات النوى، ويتم الربط عن طريق التحفيز الذاتي (autocatalytic) باحداث انشقاق داخلي أو انقسام. عادة ما يتم حجز انشقاقات التحفيز الذاتي، التي لا يشارك فيها أي بروتينات، حيث يتم حجز جزء لعمليه التشفيرللحمض النووي الريبي الرايبوسوم (rRNA)، في حين أن الانقسام الداخلي يتوافق مع اجيال الحمض النووي الريبي النقال (tRNA).
تجارب
عدلتم إجراء دراسة أجراها سيندي إل ويلز وبروس جيه دولنيك من قسم العلاجات التجريبية في معهد روزويل بارك التذكاري في بوفالو، نيويورك ومن برنامج البيولوجيا الخلوية والجزيئية بجامعة ويسكونسن في ماديسون بولاية ويسكونسن.ويسكونسن عمل على فهم العمليات الخلويه التي تشارك في النسخ الاولي. أراد الباحثون أن يفهموا ما إذا كان 5- فلورويوراسيل (FUra)، وهو دواء معروف للاستخدام في علاج السرطان، يمنع أو يوقف معالجة إنزيم ثنائي هيدروفولات (DHFR) لمعالجه ما قبل الحمض النووي الريبي الرسول (mRNA) و / أو ثبات الحمض النووي الريبي الرسول في خلايا KB المقاومة للميثوتريكسات. لم يكن للتعرض طويل المدى للـ FUra أي تأثير على مستوى DHFR قبل الحمض النووي الريبي الرسول (Pre-mRNA) الذي يحتوي على بعض الإنترونات، والتي هي من أقسام ما قبل الحمض النووي الريبي الرسول (Pre-mRNA) والتي عادة ما يتم قطعها خارج التسلسل كجزء من المعالجة. ومع ذلك، انخفضت مستويات إجمالي DHFR الحمض النووي الريبي الرسول (mRNA) إلى جزأين في الخلايا تتعرض ل 1.0 ميكرون FUra. لم يكن هناك تغيير كبير في فترة نصف العمر، مما يشير إلى الوقت الذي يستغرقه 50 ٪ من الحمض النووي الريبي الرسول (mRNA)للتحلل، من مجموع DHFR الحمض النووي الريبي الرسول أو ما قبل الحمض النووي الريبي الرسول الذي لوحظ في الخلايا المعرضة FUra. وأظهرت تجارب وضع العلامات على الحمض النووي الريبي النووي / السيتوبلازمي أن معدل الحمض النووي الريبي النووي المتغير DHFR RNA الذي يتغير إلى الحمض النووي الريبي الرسول المتغيرDHFR mRNA يقل في الخلايا التي عولجت بـ (FUra). توفر هذه النتائج أدلة إضافية على أن FUra قد تساعد في معالجة الحمض النووي الريبي الرسول و / أو تؤثر على استقرار الحمض النووي الريبي الرسول المتغيرDHFR mRNA
جوديث لينغيل وشيلدون بنمان من قسم البيولوجيا في معهد ماساتشوستس للتكنولوجيا في كامبريدج، كتبت ماساتشوستس مقالة عن نوع واحد من النسخ الأساسي الذي يشارك في جينات اثنين من ديبيرتيران dipterans ، أو الحشرات التي لها جناحان: ذبابة الفاكهة و Aedes . يصف المقال كيف نظر الباحثون في hnRNA ، أو بشكل أساسي ما قبل mRNA ، في النسخ الأولية في نوعي الحشرات. وتم نسخ حجم hnRNA وكسر hnRNA التي يتم تحويلها إلى mRNA في خطوط الخلايا، أو مجموعات من الخلايا المأخوذه من خلية واحدة من أي شيء يدرس، من Drosophila melanogaster و Aedes albopictus . كل من الحشرات ديبرتيران dipterans، ولكن Aedes لديها جينوم أكبر من ذبابة الفاكهة . وهذا يعني أن Aedes لديها المزيد من الحمض النووي، مما يعني المزيد من الجينات.Aedes تصنع خط الحمض النووي الريبي hnRNA أكبر من خط الدروسوفيلا Drosophilaعلى الرغم من أن خطي الخلية نما في ظل ظروف مماثلة وأنتجوا mRNA ناضجًا أو معالجًا بنفس الحجم وتعقيد السلاسل. تشير هذه البيانات إلى أن حجم hnRNA يزيد مع زيادة حجم الجينوم، وهو ما يظهر بوضوح من قبل Aedes.[11]
إيفو ميلكاك، ستيبانكا ميلكاكوفا، فويتك كوبسكي، ياروميرا فيكيروفا وإيفان راسكا من قسم علم الأحياء الخلوي في معهد الطب التجريبي، في أكاديمية العلوم في جمهورية التشيك في براغ، درستأثيرات البقع النووية على مرحلة Pre-mRNA . البقع النووية (البقع) هي جزء من نواة الخلايا وتخصب بعوامل الربط المعروفة للمشاركة في معالجة mRNA. لقد أظهرت البقع النووية أنها تخدم الجينات النشطة المجاورة كأماكن تخزين لعوامل الربط. في هذه الدراسة، أظهر الباحثون أنه في خلايا هيلاHeLa المأخوذه من خلايا شخص مصاب بسرطان العنق وثبت أنها مفيدة للتجارب، إن المجموعة الأولى من spliceosomesعلىpre-mRNA تأتي من هذه البقع. واستخدم الباحثون إبر دقيقة جدا من spliceosome المقبوله وadenovirus المتحوله pre-mRNAs مع عامل الربط التفاضلية لجعل مجموعات مختلفة وبعدها يتبع المواقع التي كانوا حاضرين بشكل كبير. تم استهداف Pre-mRNAs المرتبط بالسبليوزوم في البقع، ولكن وُجد أن الاستهداف يعتمد على درجة الحرارة. تشجع سلسلات polypyrimidine tract في Pre-mRNAs بناء مجموعات spliceosome واللازمة للاستهداف، لكنها في حد ذاتها ليست كافية. كانت سلاسل المرافقة مهمة بشكل خاص لاستهداف ما قبل الحمض النووي الريبي الرسول (mRNA) المتحولة في البقع. في تجارب داعمة، وسلوك البقع تبع بعد Microinjection من عقاقيرdeoxyoligoribonucleotides (سلاسل تكميلية من الحمض النووي DNA و/أو لتسلسل معين)، وفي هذه الحالة، سلاسل محدده من snRNAs . snRNAs معروف أنه الحمض النووي الريبي الذي يساعد في معالجة ما قبل الحمض النووي الريبي الرسول (mRNA). تحت هذه الظروف، مجموعات spliceosome تشكلت على ما قبل الحمض النووي الرسول (Pre-mRNA) ذاتيه النمو. وتوصل الباحثون إلى أن مجموعات spliceosome على microinjected قبل mRNA تشكل داخل البقع.يعتبر استهداف ما قبل الحمض النووي الرسول وبناءه في البقع نتيجة من تحميل عوامل الربط إلى Pre-mRNA ، ومجموعات spliceosome اعطت زياده في ملاحظه انماط البقع.[12]
الأمراض ذات الصلة
عدلقادت الأبحاث أيضًا إلى معرفة أكبر حول أمراض معينة متعلقة بالتغييرات في النسخ الاوليه. وشملت دراسة واحدة مستقبلات هرمون الاستروجين(estrogen receptors) والربط الفارق. يوضح المقال بعنوان «الربط البديل لمستقبلات هرمون الاستروجين البشري ألفا نسخة أولية: آليات تخطي الإكسون» من قبل Paola Ferro ، أليساندرا فورلاني (Alessandra Forlani)، ماركو موسيلي (Alessandra Forlani) وأولريش بفيفر (Ulrich Pfeffer) من مختبر علم الأورام الجزيئي في المعهد الوطني لأبحاث السرطان في جنوة، إيطاليا أن 1785 من النيوكليوتيدات في المنطقة في الحمض النووي (DNA) والتي تشير لمستقبلات هرمون الاستروجين ألفا (ER-alpha) تنتشر على المنطقة التي تحتوي على أكثر من 300000 من النيوكليوتيدات في النسخ الأولي. الربط بين هذا (pre-mRNA) غالبا يؤدي إلى متغيرات أو أنواع مختلفة من (mRNA) تفتقر إلى واحد أو أكثر من exons أو المناطق اللازمة لتشفير البروتينات. هذه المتغيرات ارتبطت مع تطور سرطان الثدي (breast cancer).[13] في دورة حياة retroviruses ، يتم دمج الحمض النووي (DNA) الفيروسي في نسخ من الحمض النووي (DNA)للخلية المصابة. نظرًا لأن retroviruses تحتاج إلى تغيير ما قبل الحمض النووي الريبي الرسول إلى الحمض النووي بحيث يمكن دمج هذا الحمض النووي داخل الحمض النووي المضيف الذي يؤثر عليه، إن تكوين قالب الحمض النووي هذا يعد خطوة حيوية لتكرار فيروس. نوع الخلية، واختلافها أو حالتها المتغيرة للخلية، والحالة الفسيولوجية للخلية، يؤدي إلى تغيير كبير في توافر ونشاط بعض العوامل الضروريه لعمليه النسخ. هذه المتغيرات تكون مجموعة واسعة من التعبير الجيني الفيروسي. على سبيل المثال، تحتوي خلايا الأنسجة التي تنتج بنشاط فيروسات معدية من فيروسات سرطان الدم وانفلونزا الطيور (ASLV أو MLV) تحتوي مستويات عالية من الحمض النووي الريبي الفيروسي بحيث أن 5-10 ٪ من الحمض النووي الريبي الرسول في الخلية يمكن أن تكون ذات أصل فيروسي. هذا يدل على أن النسخ الاوليه التي أنتجت من هذه الفيروسات لا تتبع دائما مسار طبيعي لإنتاج البروتين وتحول مرة أخرى إلى الحمض النووي (DNA) من أجل التكاثر والتوسع.[14]
انظر أيضًا
عدلالمراجع
عدل- ^ ا ب ج T. Strachan؛ Andrew P. Read (يناير 2004). Human Molecular Genetics 3. Garland Science. ص. 16–17. ISBN:978-0-8153-4184-0. مؤرشف من الأصل في 2014-01-03.
- ^ ا ب "Molecular Biology of the Cell". NCBI (ط. 3rd). New York: Garland Science. مؤرشف من الأصل في 2020-01-08.
- ^ "An Introduction to Genetic Analysis". NCBI. New York: W.H. Freeman. مؤرشف من الأصل في 2020-01-08.
- ^ ا ب ج Scott F. Gilbert (15 يوليو 2013). Developmental Biology. Sinauer Associates, Incorporated. ص. 38–39, 50. ISBN:978-1-60535-173-5. مؤرشف من الأصل في 2019-06-24.
- ^ "Genomes" (ط. 2nd). Wiley-Liss. مؤرشف من الأصل في 2020-01-08.
- ^ Harvey Lodish (2008). Molecular Cell Biology. W. H. Freeman. ص. 303–306. ISBN:978-0-7167-7601-7. مؤرشف من الأصل في 2014-01-03.
- ^ "Introns Protect Eukaryotic Genomes from Transcription-Associated Genetic Instability". Molecular Cell. ج. 67 ع. 4: 608–621.e6. أغسطس 2017. DOI:10.1016/j.molcel.2017.07.002. PMID:28757210.
- ^ ا ب ج د ه و ز ح ط ي "The Cell: A Molecular Approach" (ط. 2nd). Sunderland (MA): Sinauer Associates; 2000. مؤرشف من الأصل في 2020-01-08.
- ^ Weaver, Robert F. (2005). Molecular Biology, p.432-448. McGraw-Hill, New York, NY. (ردمك 0-07-284611-9).
- ^ Wahl MC، Will CL، Lührmann R (فبراير 2009). "The spliceosome: design principles of a dynamic RNP machine". Cell. ج. 136 ع. 4: 701–18. DOI:10.1016/j.cell.2009.02.009. PMID:19239890.
- ^ "hnRNA size and processing as related to different DNA content in two dipterans: Drosophila and Aedes". Cell. ج. 5 ع. 3: 281–90. يوليو 1975. DOI:10.1016/0092-8674(75)90103-8. PMID:807333.
- ^ "Prespliceosomal assembly on microinjected precursor mRNA takes place in nuclear speckles". Molecular Biology of the Cell. ج. 12 ع. 2: 393–406. فبراير 2001. DOI:10.1091/mbc.12.2.393. PMC:30951. PMID:11179423.
- ^ "Alternative splicing of the human estrogen receptor alpha primary transcript: mechanisms of exon skipping". International Journal of Molecular Medicine. ج. 12 ع. 3: 355–63. سبتمبر 2003. PMID:12883652.
- ^ Coffin JM, Hughes SH, Varmus HE, editors. Retroviruses. Cold Spring Harbor (NY): Cold Spring Harbor Laboratory Press; 1997. Available from: https://www.ncbi.nlm.nih.gov/books/NBK19441/ نسخة محفوظة 2020-09-03 على موقع واي باك مشين.