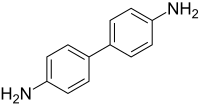
بنزيدين
بنزيدين هو مركب عضوي ينتمي إلى مجموعة ثنائيات الأمين العطرية وإلى مجموعة مركبات ثنائي الفينيل. للمركب الصيغة الكيميائية C12H12N2، والتي يمكن كتابتها على الشكل C6H4NH2)2)، ويكون على شكل بلورات صفراء محمرة.
| بنزيدين | |
|---|---|
| الاسم النظامي (IUPAC) | |
1,1'-biphenyl-4,4'-diamine |
|
| أسماء أخرى | |
Benzidine, di-phenylamine, diphenylamine, 4,4'-bianiline, 4,4'-biphenyldiamine, 1,1'-biphenyl-4,4'-diamine, 4,4'-diaminobiphenyl, p-diaminodiphenyl |
|
| المعرفات | |
| رقم CAS | 92-87-5 |
| بوب كيم (PubChem) | 7111 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C12H12N2 |
| الكتلة المولية | 184.24 غ/مول |
| المظهر | بلورات صفراء محمرة |
| الكثافة | 1.25 غ/سم3 |
| نقطة الانصهار | 127-128 °س |
| نقطة الغليان | 400 °س |
| الذوبانية في الماء | ضعيف الانحلال في الماء |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
يعد مركب البنزيدين من المواد المسرطنة.
التحضير
عدليحضر مركب البنزيدين على خطوتين من نتروبنزين؛ حيث يحول وساطياً إلى مركب 2,1-ثنائي فينيل الهيدرازين بوجود حفاز من الحديد. تؤدي معالجة المركب بالأحماض المعدنية إلى تفاعل إعادة ترتيب إلى البنزيدين؛ بالإضافة إلى تشكل متصاوغات أخرى.[3]
يعد تفاعل إعادة ترتيب البنزيدين من آليات التفاعل المثيرة للاهتمام؛[4] ويوصف التحول على أنه [5,5] تفاعل سيغماتروبي.[5][6]
الخواص
عدليوجد المركب في الشروط القياسية على شكل بلورات صفراء محمرة ضعيفة الانحلال في الماء.
للمركب خواص حيوية خطيرة فهو من المسرطنات، وخاصة سرطان المثانة؛ إذ أن مسنقلباته تشكل ناتج إضافة مع غوانين الDNA.
الاستخدامات
عدليعد مركب البنزيدين أساساً في تحضير مركبات الآزو مثل التولويدين و3،3′-ثنائي كلورو البنزيدين المستخدمة في تحضير الأصبغة مثل أحمر الكونغو.
كما كان المركب في السابق يستخدم للكشف عن وجود الدم؛ إذ كان يضاف إلى العينة بوجود بيروكسيد الهيدروجين (الماء الأكسجيني) ويعطي لون أزرق للكشف.
اقرأ أيضاً
عدلالمراجع
عدل- ^ ا ب ج BENZIDINE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Schwenecke, H.؛ Mayer, D. (2005). "Benzidine and Benzidine Derivatives". Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a03_539.
- ^ March, J. (1992). Advanced Organic Chemistry (ط. 5th). New York: J. Wiley and Sons. ISBN:0-471-60180-2. مؤرشف من الأصل في 2022-05-31.
- ^ Shine, H. J.؛ Zmuda, H.؛ Park, K. H.؛ Kwart, H.؛ Horgan, A. G.؛ Collins, C.؛ Maxwell, B. E. (1981). "Mechanism of the benzidine rearrangement. Kinetic isotope effects and transition states. Evidence for concerted rearrangement". Journal of the American Chemical Society. ج. 103 ع. 4: 955–956. DOI:10.1021/ja00394a047..
- ^ Shine, H. J.؛ Zmuda, H.؛ Park, K. H.؛ Kwart, H.؛ Horgan, A. G.؛ Brechbiel, M. (1982). "Benzidine rearrangements. 16. The use of heavy-atom kinetic isotope effects in solving the mechanism of the acid-catalyzed rearrangement of hydrazobenzene. The concerted pathway to benzidine and the nonconcerted pathway to diphenyline". Journal of the American Chemical Society. ج. 104 ع. 9: 2501–2509. DOI:10.1021/ja00373a028.