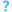ورم مخاطي (ميكسوما)
ورم مخاطي | |
|---|---|
 |
|
| تعديل مصدري - تعديل |
الورم المخاطي هو مرض يسببه فيروس الورم المخاطي (ميكسوما)، وهو من عائلة الفيروسات الجدرية من جنس فيروس جدري الأرانب. العوائل الطبيعية هي الأرنب البرازيلي (الأرنب البرازيلي قطني الذيل) في أمريكا الجنوبية والوسطى، وأرانب الفرشاة في أمريكا الشمالية. يسبب فيروس الورم المخاطي مرضًا خفيفًا فقط في هذه الأنواع، ولكنه عادةً ما يسبب مرضًا شديدًا ومميتًا في الأرانب الأوروبية. يعتبر الورم المخاطي مثالًا ممتازًا لما يحدث عندما ينتقل الفيروس من نوع يتكيف معه إلى عائل (مضيف) بسيط، وهو سبب دراسته على نطاق واسع. أُدخل الفيروس عمدًا في أستراليا وفرنسا وتشيلي في خمسينيات القرن العشرين للسيطرة على مجموعات الأرانب الأوروبية البرية.
السبب
عدلينتمي فيروس الورم المخاطي إلى جنس فيروس جدري الأرانب التابع إلى عائلة فيروسات الجدري. مثل فيروسات الجدري الأخرى، تعد فيروسات الورم المخاطي فيروسات كبيرة حاوية على شريط خطي مضاعف من الدنا (الحمض النووي الريبي منقوص الأكسجين). يحدث تنسخ الفيروس ضمن سيتوبلازم الخلية. العوائل الطبيعية هي الأرانب البرازيلية في أمريكا الجنوبية والوسطى، وأرانب الفرشاة في أمريكا الشمالية. يسبب فيروس الورم المخاطي مرضًا خفيفًا فقط في هذه الأنواع، مع أعراض تقتصر على تشكل عقيدات جلدية.[1]
الورم المخاطي هو اسم المرض الشديد والقاتل في الأرانب الأوروبية الناجم عن فيروس الورم المخاطي. توجد سلالات متنوعة تختلف في حدتها. تعد سلالة كاليفورنيا، المتفشية في الساحل الغربي للولايات المتحدة و باها في المكسيك، الأكثر حدةً، إذ بلغ معدل الإماتة 100%. تعد سلالة أمريكا الجنوبية، الموجودة في أمريكا الجنوبية وأمريكا الوسطى، أقل حدة بقليل، إذ بلغ معدل الإماتة 99.8%. أصبحت السلالات الموجودة في أوروبا وأستراليا موهنة، وبلغ معدل الإماتة 50-95%. طورت الأرانب البرية في أوروبا وأستراليا بعض المناعة ضد الفيروس، لكن هذا لا ينطبق بشكل عام على الأرانب الأليفة.[2]
الانتقال
عدلينتقل الورم المخاطي بشكل رئيسي عن طريق الحشرات. يحدث انتقال المرض عادةً عن طريق لدغات البعوض أو البرغوث، ولكن قد ينتقل أيضًا عن طريق لدغات الذباب والقمل والسوس (العنكبيات). لا يتكاثر فيروس الورم المخاطي ضمن عوائل مفصليات الأرجل هذه، وإنما ينتقل عبرها من أرنب إلى آخر. يعود سبب موسمية المرض إلى توافر المفصليات الناقلة وقرب الأرانب البرية المصابة.[3]
قد ينتقل فيروس الورم المخاطي أيضًا عن طريق الاتصال المباشر. تفرز الأرانب المصابة الفيروس في إفرازات العين والأنف ومن مناطق الجلد المتآكلة. قد يتواجد الفيروس أيضًا في السائل المنوي والإفرازات التناسلية. تعد الفيروسات الجدرية مستقرة إلى حد ما في البيئة وقد تنتشر عن طريق الأشياء الملوثة مثل زجاجات المياه أو المغذيات أو الأقفاص أو أيدي الأشخاص.[3] تعد مقاومة للجفاف ولكنها حساسة تجاه بعض المطهرات. [4]
الفيزيولوجيا المرضية
عدلأظهرت دراسة مخبرية حُقنت فيها الأرانب الأوروبية داخل الأدمة بسلالة من فيروس الورم المخاطي في أمريكا الجنوبية، التطور التالي للمرض. في البداية، تكاثر الفيروس في الجلد في موقع التلقيح. بعد يومين تقريبًا من التلقيح، وُجد الفيروس في العقد اللمفاوية القريبة، وخلال 3 أيام كان موجودًا في مجرى الدم وأعضاء البطن. بعد 4 أيام، عُزل الفيروس من الجلد غير الملقح ومن الخصيتين. لوحظت سماكة طفيفة في الأجفان ووُجد الفيروس في سائل الملتحمة في اليوم الخامس. لوحظ احتقان الخصية في اليوم السادس.[5]
التشخيص
عدلغالبًا ما يُشخص الورم المخاطي في الأرانب الأوروبية على أساس المظاهر السريرية المميزة. إذا مات أرنب دون أن تظهر عليه الأعراض الكلاسيكية للورم المخاطي، أو إذا كان هناك حاجة لمزيد من التأكيد، تتوفر مجموعة من الفحوصات المخبرية. تاريخيًا، تضمنت هذه الطرق الفحص النسيجي والفحص بالمجهر الإلكتروني وعزل الفيروس. يُظهر الفحص النسيجي للجلد المصاب عادةً خلايا اللحمة المتوسطة غير المتمايزة ضمن مصفوفة من الموسين، والخلايا الالتهابية والوذمة. يمكن رؤية مشتملات داخل السيتوبلازما في البشرة وفي ظهارة الملتحمة. يمكن أيضًا استخدام الفحص المجهري الإلكتروني بالتلوين السلبي للتشخيص بسبب الحجم الكبير والبنية المميزة لفيروسات الجدري.[6] تسمح هذه الطريقة بالتصوير السريع لفيروسات الجدري، ولكنها لا تسمح بتحديد نوع الفيروس المحدد أو المتغيرات. يبقى عزل الفيروسات «المعيار الذهبي» الذي تُقارن به طرق الكشف عن الفيروسات الأخرى.[7] من الناحية النظرية على الأقل، يمكن زرع فيروس واحد حي موجود في عينة في الخلايا المستنبتة، ما يسمح بتكاثره لإنتاج مادة كافية تتيح المزيد من التوصيف التفصيلي.[8]
أدى التطور الأحدث للطرق الجزيئية مثل تفاعل البوليميراز المتسلسل وتفاعل البوليمراز المتسلسل بالزمن الحقيقي إلى إنشاء طرق أسرع وأكثر دقة للتعرف على فيروس الورم المخاطي.[7] يعمل تفاعل البوليميراز المتسلسل بالزمن الحقيقي على تبسيط تشخيص الورم المخاطي عن طريق السماح بفحص مسحات الأنف أو العين أو الأعضاء التناسلية بسرعة. يمكن استخدامه أيضًا في عينات الأنسجة الحاوية على البارافين لتأكيد وجود فيروس الورم المخاطي وتحديد السلالة الفيروسية.[9]
العلاج
عدلفي الوقت الحالي، لا يوجد علاج نوعي للورم المخاطي. إذا اتُخذ القرار بمحاولة العلاج، تعد المراقبة الدقيقة ضرورية لتجنب المعاناة المطولة. قد تتعافى الأرانب الملقحة سابقًا أو المصابة بسلالة موهنة عند إعطائها الرعاية الداعمة بالسوائل والطعام والأدوية المضادة للفيروسات واسعة الطيف. يعتبر التوقف عن تناول الطعام والماء، وفقدان الوزن الشديد المستمر، أو انخفاض درجة حرارة المستقيم عن 37 درجة مئوية (98.6 فهرنهايت) من الأسباب التي تدعو إلى التفكير في القتل الرحيم.[3]
الوقاية
التلقيح
عدلتتوفر لقاحات ضد الورم المخاطي في بعض البلدان. تعتمد جميع اللقاحات الحية المعدلة إما على سلالات فيروس الورم المخاطي الموهن أو على فيروس الورم الليفي لشوب، والذي يوفر مناعة متصالبة. يوصى بتلقيح جميع الأرانب في مناطق العالم التي يتفشى فيها الورم المخاطي بشكل روتيني، حتى لو بقيت في الداخل، بسبب قدرة الفيروس على أن ينتقل إلى الداخل عن طريق النواقل أو أدوات العدوى. في الحالات الجماعية التي لا يتم فيها تلقيح الأرانب بشكل روتيني، يكون التطعيم في مواجهة تفشي المرض مفيدًا في الحد من الإمراضية والوفيات. لا يوفر اللقاح حماية بنسبة 100%، لذلك يجب تجنب الاتصال بالأرانب البرية والحشرات الناقلة. يجب تعديل لقاحات الورم المخاطي بانتظام لتبقى فعالة، وعادةً ما يوصى باللقاحات السنوية.
يتوفر في أوروبا والمملكة المتحدة لقاح ثنائي التكافؤ يسمى نوبيفاك ميكسو-آر إتش دي وهو يحمي من كل من الورم المخاطي ومرض نزيف الأرانب.[10] يعد هذا اللقاح مرخصًا لتمنيع الأرانب بعمر 5 أسابيع أو أكثر، إذ تستغرق بداية عملية تشكل المناعة نحو 3 أسابيع. تستمر الحماية من الورم المخاطي ومرض نزيف الأرانب لمدة 12 شهرًا، ويوصى بالتلقيح السنوي لضمان الحماية المستمرة. أُثبت أن اللقاح يحد من الوفيات ويقلل من المظاهر السريرية للورم المخاطي.[11]
التلقيح ضد الورم المخاطي محظور حاليًا في أستراليا بسبب مخاوف من أن فيروس اللقاح قد ينتشر إلى الأرانب البرية ويزيد من مناعتها ضد الورم المخاطي. نظرًا لأن الأرانب الوحشية في أستراليا تسبب بالفعل قدرًا كبيرًا من الأضرار البيئية، تأخذ الحكومة هذا القلق على محمل الجد.[12] يستمر موت العديد من الأرانب الأليفة في أستراليا نتيجة الورم المخاطي بسبب افتقارها إلى المناعة.[13] هناك حملة واحدة على الأقل للسماح بتلقح الحيوانات الأليفة.[14] تدعم الجمعية الأسترالية البيطرية تقديم لقاح آمن وفعال للورم المخاطي للأرانب الأليفة،[15] ودعت الجمعية الملكية لمنع القسوة على الحيوانات الأسترالية مرارًا وتكرارًا إلى مراجعة لقاحات فيروس الورم المخاطي المتاحة وإجراء تقييم علمي لتأثيراتها المحتملة في البيئة الأسترالية.[16]
المراجع
عدل- ^ Meredith، A (2013). "Viral skin diseases of the rabbit". Veterinary Clinics of North America: Exotic Animal Practice. ج. 16 ع. 3: 705–714. DOI:10.1016/j.cvex.2013.05.010. PMID:24018033.
- ^ Kerr، P (2017). "Genomic and phenotypic characterization of myxoma virus from Great Britain reveals multiple evolutionary pathways distinct from those in Australia". PLOS Pathogens. ج. 13 ع. 3: e1006252. DOI:10.1371/journal.ppat.1006252. PMC:5349684. PMID:28253375.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ ا ب ج Kerr، P (2013). "Viral Infections of Rabbits". Veterinary Clinics of North America: Exotic Animal Practice. ج. 16 ع. 2: 437–468. DOI:10.1016/j.cvex.2013.02.002. PMC:7110462. PMID:23642871.
- ^ "Disinfection". The Center for Food Security and Public Health. مؤرشف من الأصل في 2020-10-24. اطلع عليه بتاريخ 2019-07-21.
- ^ Fenner، F؛ Woodroofe، GM (1953). "The pathogenesis of infectious myxomatosis: the mechanism of infection and the immunological response in the European rabbit (Oryctolagus cuniculus)". The British Journal of Experimental Pathology. ج. 34 ع. 4: 400–411. PMC:2073564. PMID:13093911.
- ^ Quesenberry، K (2012). Ferrets, Rabbits, and Rodents: Clinical Medicine and Surgery (ط. Third). Elsevier Saunders. ص. 240. ISBN:978-1-4160-6621-7. مؤرشف من الأصل في 2021-02-27.
- ^ ا ب MacLachlan، J (2017). Fenner's Veterinary Virology, 5th Edition. Elsevier. ص. 158. ISBN:978-0-12-800946-8.
- ^ MacLachlan، J (2017). Fenner's Veterinary Virology, 5th Edition. Elsevier. ص. 112. ISBN:978-0-12-800946-8.
- ^ Albini، S؛ Sigrist، B؛ Güttinger، R؛ وآخرون (6 ديسمبر 2011). "Development and validation of a real-time polymerase chain reaction assay" (PDF). Journal of Veterinary Diagnostic Investigation. ج. 24 ع. 1: 135–137. DOI:10.1177/1040638711425946. PMID:22362943. S2CID:32171325. مؤرشف من الأصل (PDF) في 2021-03-08.
- ^ "Nobivac Myxo RHD". MSD Animal Health. مؤرشف من الأصل في 2019-07-20. اطلع عليه بتاريخ 2019-07-20.
- ^ "Nobivac Myxo RHD Data Sheet". European Medicine Agency. مؤرشف من الأصل في 2019-07-20. اطلع عليه بتاريخ 2019-07-20.
- ^ "A Statement from the Chief Veterinary Officer (Australia) on myxomatosis vaccine availability in Australia". Australian Government Department of Agriculture. مؤرشف من الأصل في 2021-03-03. اطلع عليه بتاريخ 2019-07-20.
- ^ "The Rabbit Sanctuary Myxomatosis Hotline". Myxomatosis. مؤرشف من الأصل في 2021-03-26. اطلع عليه بتاريخ 2019-07-20.
- ^ "Myxo Campaign". Myxomatosis. مؤرشف من الأصل في 2021-03-26. اطلع عليه بتاريخ 2019-07-20.
- ^ "Myxomatosis vaccination of pet rabbits". Australian Veterinary Association. مؤرشف من الأصل في 2021-03-11. اطلع عليه بتاريخ 2019-07-20.
- ^ "Why can't I vaccinate my rabbit against Myxomatosis?". Royal Society for the Prevention of Cruelty to Animals. مؤرشف من الأصل في 2021-06-04. اطلع عليه بتاريخ 2019-07-20.
| ورم مخاطي في المشاريع الشقيقة: | |
| |