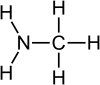
ميثيل أمين
ميثيل أمين هو مركب عضوي صيغتة CH3NH2. هذا الغاز عديم اللون هو مشتق من الأمونيا ، ولكن مع استبدال ذرة الهيدروجين بمجموعة الميثيل . إنه أبسط أمين أساسي . يباع كمحلول في الميثانول ، أو الإيثانول ، أو رباعي هيدروفيوران ، أو الماء ، أو كغاز لا مائي في الحاويات المعدنية المضغوطة. صناعيًا ، يتم نقل ميثيل أمين في شكله اللامائي في عربات السكك الحديدية ومقطورات الصهريج المضغوطة. له رائحة قوية مشابهة للأسماك. يستخدم الميثيل أمين ككتلة بناء لتركيب العديد من المركبات الأخرى المتاحة تجاريا.
| ميثيل أمين | |
|---|---|
 |
 |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Methanamine[بحاجة لمصدر] |
|
| أسماء أخرى | |
|
|
| المعرفات | |
| الاختصارات | MMA |
| رقم CAS | 74-89-5 |
| بوب كيم (PubChem) | 6329 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | CH5N |
| كتلة مولية | 31.06 غ.مول−1 |
| المظهر | غاز عديم اللون |
| الرائحة | شبيهة بالسمك والأمونيا |
| الكثافة | 656.2 كغم·م−3 (25 °س) |
| نقطة الانصهار | -93 °س، 180.05 °ك، -136 °ف |
| نقطة الغليان | -7--6 °س، 266.5-267.1 °ك، 20-21 °ف |
| الذوبانية في الماء | 1.08 كغم·ل−1 (20 °س) |
| log P | −0.472 |
| ضغط البخار | 186.10 كيلوباسكال (20 °س) |
| قه | 1.4 نانومول·باسكال−1·كغم−1 |
| حموضة (pKa) | 10.62 [1] |
| القاعدية (pKb) | 3.36 |
| قابلية مغناطيسية | -27.0×10−6 سم3/مول |
| اللزوجة | 230 مايكروباسكال·ثا (0 °س) |
| عزم جزيئي ثنائي القطب | 1.31 ديباي |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
−23.5 كيلوجول·مول−1 |
| المخاطر | |
| رمز الخطر وفق GHS |    |
| وصف الخطر وفق GHS | DANGER |
| بيانات الخطر وفق GHS | H220, H315, H318, H332, H335 |
| بيانات وقائية وفق GHS | P210, P261, P280, P305+351+338, P410+403 |
| NFPA 704 |
|
| حدود الاشتعال | 4.9–20.7% |
| حد التعرض المسموح به U.S | 10 جزء في المليون (12 مغ/م3) (TWA)[2] |
| LD50 | 100 مغ·كغم−1 (فموي, فأر) |
| مركبات متعلقة | |
| ألكانات أمين ذات علاقة | إيثيل أمين، ثنائي ميثيل أمين، ثلاثي ميثيل أمين |
| مركبات ذات علاقة | أمونيا |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الإنتاج الصناعي
عدليتم تحضير الميثيل أمين تجاريا بواسطة تفاعل الأمونيا مع الميثانول في وجود محفز ألومينوسيليكات. يتم إنتاج ثنائي ميثيل أمين وثلاثي ميثيل أمين بشكل مشترك. تحدد حركية التفاعل ونسب المتفاعل نسبة المنتجات الثلاثة. المنتج الأكثر تفضيلاً من قبل حركية التفاعل هو ثلاثي ميثيل أمين.[3]
CH3OH + NH3 → CH3NH2 + H2O وبهذه الطريقة ، تم إنتاج ما يقدر بـ 115،000 طن في عام 2005.[4]
طرق مخبرية
عدلتم تحضير الميثيل أمين لأول مرة في عام 1849 من قبل تشارلز أدولف وورتز عن طريق التحلل المائي لميثيل أيزوسيانات والمركبات ذات الصلة.[4][5] مثال على هذه العملية يتضمن استخدام إعادة ترتيب هوفمان ، لإعطاء الميثيل أمين من اسيلامايد وغاز البروم [6][7]
.
في المختبر ، يتم إعداد هيدروكلوريد الميثيل أمين بسهولة عن طريق وسائل أخرى مختلفة. تستلزم طريقة واحدة علاج الفورمالديهايد مع كلوريد الأمونيوم.[8]
NH4Cl + H2CO → [CH2 = NH2] Cl + H2O [CH2 = NH2] Cl + H2CO + H2O → [CH3NH3] Cl + HCO2H يمكن تحويل ملح هيدروكلوريد عديم اللون إلى أمين عن طريق إضافة قاعدة قوية ، مثل هيدروكسيد الصوديوم (NaOH):
[CH3NH3] Cl + NaOH → CH3NH2 + NaCl + H2O ينطوي أسلوب آخر على تقليل النيتروميتان مع الزنك وحمض الهيدروكلوريك.
وهناك طريقة أخرى لإنتاج الميثيل أمين هي نزع الكربوكسيل التلقائي من الجليسين مع وجود قاعدة قوية في الماء.[9]
التفاعل والتطبيقات
عدلالميثيل أمين هو نيوكليوفيل جيد.[10] كأمين يعتبر قاعدة ضعيفة. استخدامه في الكيمياء العضوية منتشر. تتضمن بعض التفاعلات التي تتضمن كواشف بسيطة: مع الفوسجين إلى إيزوسيانات الميثيل ، مع ثاني كبريتيد الكربون وهيدروكسيد الصوديوم إلى ميثيل دايثوكرباميت الصوديوم ، مع الكلوروفورم والقاعدة إلى ميثيل أيزوسيانيد ومع أكسيد الإيثيلين إلى ميثيل إيثانول أمين. يحتوي ميثيل أمين السائل على خصائص مذيبة مماثلة لتلك الخاصة بالأمونيا السائلة.[11]
وتشمل المواد الكيميائية ذات الأهمية التجارية الكبيرة والمنتجة من ميثيل أمين الأدوية المحتوية على الإيفيدرين والثيوفيللين ، ومبيدات الآفات الكاربوفيوران ، والكرباريل ، وميثام الصوديوم ، و بعض المذيبات . يتطلب تحضير بعض المواد الخافضة للتوتر السطحي ومطوري الصور الفوتوغرافية وجود ميثيل أمين ككتلة بناء.[4]
الكيمياء البيولوجية
عدلينشأ الميثيل أمين نتيجة للتعفن وهو مادة أساس لتكوُّن الميتان.[12] بالإضافة إلى ذلك ، يتم إنتاج ميثيل امين خلال ازالة مجموعة ميثل أرجينين المعتمدة على PADI4.[13]
السلامة
عدلالجرعة المميتة على الفأر هي 2.5 غ / كغ [14]
.
حددت إدارة السلامة والصحة المهنية (OSHA) والمعهد الوطني للسلامة والصحة المهنيتين (NIOSH) حدود التعرض المهني عند 10 جزء في المليون أو 12 ملغم / م 3 على مدار 8 ساعات مرجح زمني.[15]
ضبط
عدلفي الولايات المتحدة ، يتم التحكم في الميثيل أمين كمواد كيميائية من القائمة 1 من قبل إدارة مكافحة المخدرات [16] بسبب استخدامها في الإنتاج غير المشروع للميثامفيتامين.[17]
مراجع
عدل- ^ H. K. Hall (1957-10). "Correlation of the Base Strengths of Amines 1". Journal of the American Chemical Society (بالإنجليزية). 79 (20): 5441–5444. DOI:10.1021/JA01577A030. ISSN:0002-7863. QID:Q23571040.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|publication-date=(help) - ^ "NIOSH Pocket Guide to Chemical Hazards #0398". المعهد الوطني للسلامة والصحة المهنية (NIOSH).
- ^ Corbin D.R.؛ Schwarz S.؛ Sonnichsen G.C. (1997). "Methylamines synthesis: A review". Catalysis Today. ج. 37 ع. 24: 71–102. DOI:10.1016/S0920-5861(97)00003-5.
- ^ ا ب ج Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke "Amines, Aliphatic" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. دُوِي:10.1002/14356007.a02_001
- ^ Charles-Adolphe Wurtz (1849) "Sur une série d'alcalis organiques homologues avec l'ammoniaque" (On a series of homologous organic alkalis containing ammonia), Comptes rendus … , 28 : 223-226. Note: Wurtz's empirical formula for methylamine is incorrect because chemists in that era used an incorrect atomic mass for carbon (6 instead of 12). نسخة محفوظة 07 فبراير 2016 على موقع واي باك مشين.
- ^ Mann، F. G.؛ Saunders، B. C. (1960). Practical Organic Chemistry, 4th Ed. London: Longman. ص. 128. ISBN:9780582444072. مؤرشف من الأصل في 2018-09-15.
- ^ Cohen، Julius (1900). Practical Organic Chemistry 2nd Ed. London: Macmillan and Co., Limited. ص. 72. مؤرشف من الأصل في 2020-04-12.
- ^ Marvel, C. S.; Jenkins, R. L.(1941)."Methylamine Hydrochloride". Org. Synth.; Coll. Vol. 1: 347.
- ^ Gatterman, Ludwig؛ Wieland, Heinrich (1937). Laboratory Methods of Organic Chemistry. Edinburgh, UK: R & R Clark, Limited. ص. 157–158. مؤرشف من الأصل في 2020-04-12.
{{استشهاد بكتاب}}: الوسيط غير المعروف|last-author-amp=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Peter Scott (المحرر). Linker Strategies in Solid-Phase Organic Synthesis. ص. 80. مؤرشف من الأصل في 2020-04-12.
...an unhindered amine such as methylamine
- ^ Debacker، Marc G.؛ Mkadmi، El Bachir؛ Sauvage، François X.؛ Lelieur، Jean-Pierre؛ Wagner، Michael J.؛ Concepcion، Rosario؛ Kim، Jineun؛ McMills، Lauren E. H.؛ Dye، James L. (1996). "The Lithium−Sodium−Methylamine System: Does a Low-Melting Sodide Become a Liquid Metal?". Journal of the American Chemical Society. ج. 118 ع. 8: 1997. DOI:10.1021/ja952634p.
- ^ Thauer، R. K. (1998). "Biochemistry of methanogenesis: A tribute to Marjory Stephenson:1998 Marjory Stephenson Prize Lecture". Microbiology. ج. 144 ع. 9: 2377–406. DOI:10.1099/00221287-144-9-2377. PMID:9782487.
- ^ Ng، SS؛ Yue، WW؛ Oppermann، U؛ Klose، RJ (فبراير 2009). "Dynamic protein methylation in chromatin biology". Cellular and molecular life sciences : CMLS. ج. 66 ع. 3: 407–22. DOI:10.1007/s00018-008-8303-z. PMC:2794343. PMID:18923809.
- ^ The Merck Index, 10th Ed. (1983), p.864, Rahway: Merck & Co.
- ^ CDC - NIOSH Pocket Guide to Chemical Hazards نسخة محفوظة 19 ديسمبر 2017 على موقع واي باك مشين.
- ^ Title 21 Code of Federal Regulations نسخة محفوظة 17 أكتوبر 2017 على موقع واي باك مشين.
- ^ Frank، R. S (1983). "The Clandestine Drug Laboratory Situation in the United States". Journal of Forensic Sciences. ج. 28: 12235J. DOI:10.1520/JFS12235J.
| في كومنز صور وملفات عن: ميثيل أمين |