رباعي أكسيد الزينون
رباعي أكسيد الزينون هو مركب كيميائي من زينون والأكسجين، صيغته الجزيئية (XEO 4)، ويعد المركب مستقرا نسبيا للغازات النبيلة. المركب صلب بلوري أصفر اللون، مستقر تحت 935.9 درجة مئوية؛ وفوق درجة الحرارة هذه يكون عرضة للانفجار والتحلل إلى عنصري الزينون وأكسجين (O2).
| رباعي أكسيد الزينون | |
|---|---|
 |
 |
| الاسم النظامي (IUPAC) | |
Xenon tetraoxide |
|
| أسماء أخرى | |
Xenon tetroxide |
|
| المعرفات | |
| رقم CAS | 12340-14-6 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | XeO4 |
| الكتلة المولية | 195.29 g mol−1 |
| المظهر | Yellow solid below −36 °C |
| الكثافة | ? g cm−3, solid |
| نقطة الانصهار | −35.9 °س، 237 °ك، -33 °ف |
| نقطة الغليان | 0 °س، 273 °ك، 32 °ف |
| البنية | |
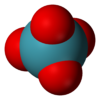
| البنية الجزيئية | بنية جزيئية رباعية السطوح[1] |
| عزم جزيئي ثنائي القطب | 0 D |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
+153.5 kcal mol−1 [2] |
| إنتروبيا مولية قياسية S |
? J.K−1.mol−1 |
| المخاطر | |
| ترميز المخاطر | Explosive (E) |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
جميع الإلكترونات التكافؤ الثمانية من الزينون مرتبطة في الروابط مع الأكسجين ، وحالة أكسدة ذرة الزينون هي +8. الأكسجين هو العنصر الوحيد الذي يمكن أن يحقق الزينون لأعلى حالة أكسدة ؛ حتى الفلور يمكن أن يعطي فقط XeF 6 (+6). يمكن الوصول إلى اثنين من مركبات الزينون الأخرى قصيرة العمر مع حالة أكسدة +8 ، XeO 3 F 2 و XeO 2 F 4 ، من خلال تفاعل رباعي أكسيد الزينون مع سداسي فلوريد الزينون . XeO 3 F 2 و XeO 2 F 4 يمكن الكشف عنها مع مطياف الكتلة . و perxenates هي المركبات أيضاً حيث زينون لديه حالة +8 الأكسدة.
التفاعلات الكيميائية
عدلعند درجات حرارة أعلى من 35.9 درجة مئوية ، يكون رباعي أكسيد الزينون معرضاً للانفجار ويتحلل إلى غاز الأكسجين والأكسجين باستخدام ΔH = −643 kJ / mol:
- XeO4 → Xe + 2 O2
يذوب رباعي أكسيد الزينون في الماء ليشكل حمض بيركسينيك وفي القلويات لتشكيل أملاح بيركسينات:
- XeO4 + 2 H2O → H4XeO6
- XeO4 + 4 NaOH → Na4XeO6 + 2 H2O
رباعي أكسيد الزينون يمكن أن يتفاعل أيضًا مع سداسي فلوريد الزينون لإعطاء أوكسين فلوريد:
- XeO4 + XeF6 → XeOF4 + XeO3F2
- XeO4 + 2XeF6 → XeO2F4 + 2 XeOF4
مراجع
عدل- ^ G. Gundersen؛ K. Hedberg؛ J. L.Huston (1970). "Molecular Structure of Xenon Tetroxide, XeO4". J. Chem. Phys. ج. 52 ع. 2: 812–815. DOI:10.1063/1.1673060.
- ^ Gunn، S. R. (مايو 1965). "The Heat of Formation of Xenon Tetroxide". Journal of the American Chemical Society. ج. 87 ع. 10: 2290–2291. DOI:10.1021/ja01088a038.
| رباعي أكسيد الزينون في المشاريع الشقيقة: | |
| |