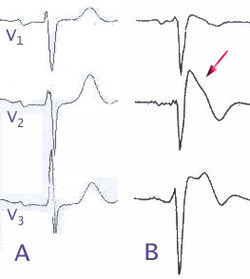
متلازمة بروغادا
متلازمة بروغادا هي اضطراب وراثي يكون فيه النشاط الكهربائي للقلب غير طبيعي،[2] ويزيد من خطر حدوث اضطراب النظم القلبي والموت القلبي المفاجئ.[2] وقد يعاني المتضررون من نوبات إغماء.[2] وغالبًا ما تحدث اضطرابات نظم القلب المصاحبة لمتلازمة بروغادا أثناء الراحة كما قد تحدث بسبب الحمى.[1][5]
| متلازمة بروغادا | |
|---|---|
A) تخطيط طبيعي لكهربائية القلب
B) متغيرات تخطيط كهربائية القلب في متلازمة بروغادا
| |
| تسميات أخرى | متلازمة موت القلب الفجائي الليلي الغير مفسر [1] |
| معلومات عامة | |
| الاختصاص | طب القلب |
| من أنواع | إحصار القلب، ومتلازمة الموت المفاجئ، ومرض |
| الأسباب | |
| الأسباب | جينات، أدوية[2] |
| عوامل الخطر | إصابة أحد أفراد العائلة، العرق الآسوي، الذكور [1][2] |
| المظهر السريري | |
| البداية المعتادة | مرحلة البلوغ[2] |
| الأعراض | الإغماء، توقف القلب[2] |
| الإدارة | |
| التشخيص | تخطيط كهربائية القلب، اختبارات جينية[2][3] |
| العلاج | الانتظار والمشاهدة، مقوم نظم القلب مزيل الرجفان القابل للزرع، أدوية (ICD)[3][4] |
| حالات مشابهة | متلازمة رومانو-وارد، اعتلال عضلة القلب، حثل عضلي دوشيني[3] |
| الوبائيات | |
| انتشار المرض | 5 في كل 10,000[1] |
| الوفيات | 8% of توقف القلب[2] |
| تعديل مصدري - تعديل | |
لدى حوالي ربع المصابين بمتلازمة بروغادا فرد في الأسرة مصاب بها كذلك.[2] وقد تكون بعض الحالات بسبب طفرة وراثية جديدة أو بسبب بعض الأدوية،[1] ويُعتبر الجين الأكثر شيوعا هو جين قناة الصوديوم NAV1.5 الذي يشفر قنوات الصوديوم الموجودة في القلب.[6] يتم تشخيص المتلازمة عادة باستخدام تخطيط كهربائية القلب، ومع ذلك فقد قد لا يكون اضطراب القلب الكهربي موجود باستمرار.[2] ويمكن استخدام بعض الأدوية مثل الأجملين لإظهار هذه الاضطرابات في تخطيط كهربائية القلب.[2] وقد تظهر أنماط مماثلة لهذه الاضطرابات في بعض اضطرابات الكهرل أو عندما يحدث نقص في تدفق الدم إلى القلب.[7]
لا يوجد في الوقت الحالي شفاء لمتلازمة بروغادا.[3] إلا أنه يمكن التعامل مع أولئك المعرضين لخطر موت القلب المفاجئ باستخدام مقوم نظم القلب مزيل الرجفان القابل للزرع.[4] وبالنسبة لأولئك الذين ليس لديهم أعراض فإن خطر الوفاة يكون أقل بكثير، أما كيفية علاجهم فهو أمر أقل وضوحًا.[3][8] ويمكن استخدام الايزوبروترينول على المدى القصير لأولئك الذين لديهم إيقاعات قلب غير طبيعية تهدد الحياة بشكل متكرر، بينما يمكن استخدام الكوينيدين على المدى الطويل،[3][9] وقد يُوصى الطبيب بفحص أفراد أسرة المصاب.[3]
تصيب متلازمة بروغادا ما بين 1 إلى 30 في كل 10000 شخص.[2] وهي أكثر شيوعًا في الذكور عن الإناث، كما أنها أكثر شيوعا في ذوي الأصول الآسيوية.[1][2] وتظهر أعراضها عادة في مرحلة البلوغ.[2] وقد سميت المتلازمة بهذا الاسم نسبة إلى أخصائي القلب الإسبانيين وهم بيدرو بروغادا وجوسيب بروغادا اللذين وصفا الحالة عام 1992.[3][10] وشقيقهم رامون بروغادا أول من وصف أحد الأسباب الوراثية المحتملة عام 1998.[11]
العلامات والأعراض عدل
في حين أن العديد من المصابين بمتلازمة بروغادا ليس لديهم أية أعراض، إلا أن متلازمة بروغادا قد تسبب الإغماء أو الموت القلبي المفاجئ بسبب اضطرابات نظم القلب الخطيرة مثل الرجفان البطيني أو تسرع القلب البطيني،[8] وتكون هذه الاضطرابات هي سبب الإغماء، والتي تعود إلى النظم الطبيعي مجددا بشكل تلقائي. في حالة ما إذا لم يتوقف اضطراب نظم القلب من تلقاء نفسه وتُرك دون تناول علاج، فقد يصاب الشخص بسكتة قلبية قاتلة، ومع ذلك فإن الإغماء يمكن أن يحدث في المصابين بمتلازمة بروغادا حتى عند غياب اضطرابات نظم القلب، وذلك بسبب انخفاض ضغط الدم المفاجئ، بسبب يُعرف باسم الاستجابة الوعائية المبهمية.[2]
غالبًا ما تحدث اضطرابات نظم القلب التي تظهر في متلازمة بروغادا أثناء الراحة أو بعد تناول وجبة ثقيلة أو حتى أثناء النوم.[5] وهي حالات يحدث فيها تنشيط للعصب المبهم، وتُعرف باسم «فترات زيادة نغمة العصب المبهم». وقد تحدث اضطرابات نظم القلب أيضًا أثناء الحمى أو بعد تناول الكحوليات بشكل مفرط، كما قد تؤدي بعض الأدوية أيضًا إلى تفاقم هذه الاضطرابات وبالتالي يجب علي المصابين تجنبها.[12]
الأسباب عدل
تتواصل خلايا القلب المفردة مع بعضها البعض عبر إشارات كهربائية، وهذه الإشارات الكهربائية تكون متعطلة في المصابين بمتلازمة بروغادا، وباعتبارها حالة وراثية فإن سبب هذه المتلازمة في نهاية المطاف هو تغييرات في الحمض النووي للشخص المصاب، والمعروفة باسم الطفرات الوراثية، وقد كانت أولى الطفرات المصاحبة لمتلازمة بروغادا موصوفة في جين مسؤول عن بروتين أو قناة أيونية تتحكم في تدفق أيونات الصوديوم عبر غشاء خلايا عضلة القلب (قنوات الصوديوم القلبية). وتؤثر العديد من الطفرات الوراثية التي وصفت لاحقا على أنها مصاحبة لمتلازمة بروغادا على تيار الصوديوم بطريقة ما، أو تؤثر على التيارات الأيونية الأخرى. [7]
وُصفت قائمة طويلة للعوامل التي يمكن أن تولد نمط تخطيط قلبي مماثل لتخطيط بروغادا، وشملت القائمة اضطرابات الكهرل مثل انخفاض مستويات البوتاسيوم في الدم، وانخفاض إمدادات الدم إلى المناطق الرئيسية في القلب وتحديدا مسار التدفق البطيني الأيمن،[7] وبعض الأدوية مثل مضادات اضطراب النظم مثل فليكاينيد وفيراباميل وبروبرانولول، ومضادات الاكتئاب مثل أميتربتيلين، والعقاقير التي تزيد من تأثير العصب المبهم مثل الأستيل كولين. كما يمكن أيضًا رؤية نمط تخطيط مماثل لتخطيط بروغادا عقب التناول المفرط للكحول أو الكوكايين. [7]
علم الوراثة عدل
تورث متلازمة بروغادا بطريقة السيادة الجسدية، مما يعني أن وجود نسخة واحدة فقط من الجين المعيب يمكن أن تسبب في حدوث المتلازمة، ومع ذلك فإن المصاب بالمتلازمة قد يكون أول شخص في عائلته يصاب بها إذا نشأت كطفرة جديدة.[5] ويُعرف الجين الذي توجد فيه الطفرات بشكل شائع في متلازمة بروجادا باسم SCN5A، وهو المسؤول عن قنوات الصوديوم القلبية، حيث تتسبب طفرات هذا الجين المصاحبة لمتلازمة بروجادا عمومًا في انخفاض تدفق أيونات الصوديوم. ومع ذلك فإن 20 ٪ فقط من حالات متلازمة بروغادا يصاحبها طفرات في هذا الجين، حيث أن الاختبارات الجينية لغالبية المصابين بمتلازمة بروغادا غير قادرة على تحديد الطفرة الجينية المسؤولة.[5] وقد تم اكتشاف أكثر من 290 طفرة في هذا الجين حتى الآن، كل منها يغير من وظيفة قنوات الصوديوم بطريقة مهارية مختلفة.[13] وهذا الاختلاف يفسر جزئيًا التباين في شدة الحالة بين المصابين، بدءًا من كونها حالة خطيرة للغاية تسبب الوفاة في سن مبكرة، إلى كونها حالة حميدة قد لا تسبب أي مشاكل على الإطلاق. ومع ذلك فإن وراثة متلازمة بروغادا هي أمر معقد، ومن المحتمل أن تكون المتلازمة ناتجة عن تفاعل بين العديد من الجينات، وبسبب هذا التفاعل المعقد قد يُظهر بعض أفراد الأسرة الحاملين لطفرة معينة أدلة على إصابتهم بمتلازمة برغادا، في حين لا يُظهر الآخرون الحاملون لنفس الطفرة أي أدلة، ويشار إلى ذلك باسم النفوذية المتباينة.[14]
تم تحديد عدة جينات أخرى مصاحبة لمتلازمة بروجادا، بعض هذه الجينات مسؤول عن البروتينات الأخرى التي تشكل جزءًا من قناة الصوديوم، والمعروفة باسم وحدات بيتا الفرعية لقناة الصوديوم، وشكلت بعض الجينات الأخرى أنواعًا مختلفة من قنوات الصوديوم، فيما قامت بعض هذه الجينات بحمل شفرة القنوات الأيونية التي تحمل أيونات الكالسيوم أو البوتاسيوم،[15] وولدت بعض الجينات الأخرى بروتينات تتفاعل مع القنوات الأيونية، وتتضمن الجينات المصاحبة لمتلازمة بروغادا ووصفها ما يلي:
| النوع | OMIM | جينة | ملاحظات |
|---|---|---|---|
| BrS1 | 601144 | SCN5A | الوحدة الفرعية Na V 1.5 - α لقناة الصوديوم القلبية تحمل تيار الصوديوم I Na . [6] |
| BrS2 | 611778 | GPD1L | هيدروجيناز الجلسرين -3 فوسفات مثل الببتيد - انخفاض نشاط GPD1-L يؤدي إلى الفسفرة من Na V 1.5 وانخفاض I Na . [6] |
| BrS3 | 114205 | CACNA1C | Ca <sub id="mwdw">V</sub> 1.2 - α وحدة فرعية من قناة الكالسيوم التي تعتمد على الجهد تحمل تيار الكالسيوم L- نوع I Ca (L).[16] |
| BrS4 | 600003 | CACNB2 | الوحدة الفرعية Ca V β2B - β-2 لقناة الكالسيوم ذات الجهد الكهربائي والتي تحمل تيار الكالسيوم من النوع L I I (L) . [16] |
| BrS5 | 600235 | SCN1B | الوحدة الفرعية Na V β1 - 1-1 لقناة الصوديوم التي تحمل تيار الصوديوم I Na . [16] |
| BrS6 | 604433 | KCNE3 | MiRP2 - β وحدة فرعية لقنوات البوتاسيوم ذات الجهد الكهربائي. يعدل من البوتاسيوم الخارج عابر الحالي الأول ل . [16] |
| BrS7 | 608214 | SCN3B | الوحدة الفرعية Na V β3 - β-3 لقناة الصوديوم القلبية التي تحمل تيار الصوديوم I Na . [6] |
| BrS8 | 600935 | KCNJ8 | Kir6.1، يحمل البوتاسيوم المعدل الحالي I Kir . [6] |
| BrS9 | 114204 | CACNA2D1 | الوحدة الفرعية α2δ لقناة الكالسيوم ذات الجهد الكهربائي والتي تحمل تيار الكالسيوم من النوع L I I (L) . [6] |
| BrS10 | 605411 | KCND3 | K V 4.3، ألفا- فرعية للقناة البوتاسيوم الخارج عابرة I ل. [6] |
| BrS11 | 607954 | RANGRF | يشفر MOG1 - يؤثر على الاتجار في Na V 1.5. [6] |
| BrS12 | 602701 | SLMAP | يؤثر البروتين المرتبط بغشاء Sarcolemmal ، وهو مكون من الأنابيب التائية والشبكة الساركوبلازمية - على تهريب Na V 1.5. [6] |
| BrS13 | 601439 | ABCC9 | SUR2A ، ناقل شرائط كاسيت ثلاثي الأدينوسين (ATP) ملزم لقناة I K (ATP) . [6] |
| BrS14 | 601327 | SCN2B | Na V β2 - وحدة بيتا -2 الفرعية لقناة الصوديوم القلبية تحمل تيار الصوديوم I Na . [6] |
| BrS15 | 602861 | PKP2 | Plakophillin-2 - يتفاعل مع I Na . [6] |
| BrS16 | 601513 | FGF12 | عامل نمو الخلايا الليفية مثلي عامل -1 - طفرة يقلل أنا نا . [6] |
| BrS17 | 604427 | SCN10A | الوحدة الفرعية Na <sub id="mw-w">V</sub> 1.8 - α من قناة الصوديوم العصبية. [16] |
| BrS18 | 604674 | HEY2 | عامل النسخ المحدد في دراسة الارتباط على نطاق الجينوم. [6] |
| BrS19 | 603961 | SEMA3A | Semaphorin. [6] |
| BrS20 | 601142 | KCNAB2 | K V β2 ، قناة البوتاسيوم ذات الجهد الكهربي un2 وحدة فرعية - طفرة تزيد من I إلى . [16] |
يمكن لبعض الطفرات المصاحبة لمتلازمة بروغادا يمكن أن تسبب أمراض قلبية أخرى. ويُوصف أولئك الذين يعانون من أكثر من حالة قلبية واحدة في نفس الوقت بسبب نفس الطفرة بأنهم يعانون من «المتلازمة المتراكبة» التي يشمل أحد أمثلتها تراكب كل من متلازمة بروغادا ومتلازمة كيو تي الطويلة، والتي تسببها طفرة في جين SCN5A مما يقلل من ذروة تيار الصوديوم ولكنه في الوقت نفسه يترك تسرب مستمر.[7] كذلك وُصفت متلازمة بروغادا بأنها متراكبة مع خلل تنسج البطين الأيمن المحدث لاضطراب النظم بسبب طفرة في جين PKP2، مما يُسبب نمط تخطيط قلب مماثل لنمط بروغادا مع تغييرات هيكلية مميزة لخلل تنسج البطين الأيمن المحدث لاضطراب النظم.[17]
آلية العمل عدل
يلاحظ في متلازمة بروغادا أن اضطراب نظم القلب يأخذ أنماطا خطيرة مثل الرجفان البطيني أو تسارع القلب البطيني المتعدد الأشكال، وقد يعاني المصابين بالمتلازمة من تسارع القلب الناتج عن اضطرابات نظم القلب الأقل خطورة مثل تسرع القلب بسبب إعادة الدخول بالعقدة الأدينية البطينية[18] أو تباطئ غير طبيعي للقلب مثل متلازمة العقدة الجيبية المريضة.[19] وهناك العديد من الآليات التي تسبب من خلالها الطفرات الجينية هذه الحالات التي تتسبب في اضطراب نظم القلب.[20]
يجادل البعض في أن السبب الرئيسي وراء نشوء هذه الاضطراب النظمية هو التوصيل الكهربائي البطيء لمناطق القلب بشكل غير طبيعي، وبالتحديد البطين الأيمن، وتدعم المتغيرات الوراثية المصاحبة لمتلازمة بروغادا مفهوم أن جين SCN5A (وهو الجين الأكثر شيوعًا في المتلازمة) وكذلك الجينات SCN10A و SCN1B و SCN2B و SCN3B كلها تؤثر بشكل مباشر على تيار الصوديوم، حيث يُعتبر تيار الصوديوم مساهماً رئيسياً في التدفق المميز للشحنة الكهربائية التي تحدث مع كل نبضة قلبية عبر غشاء الخلايا القلبية والمعروفة باسم جهد الفعل القلبي، ويؤدي تيار الصوديوم إلى حدوث ضربة مبدئية سريعة لجهد الفعل (المرحلة 0)، وتقليل ذروة التيار المبكرة، كما يؤدي إلى تباطؤ التوصيل الكهربائي عبر عضلة القلب فقط عند وجود المتغيرات الوراثية المصاحبة لمتلازمة بروغادا،[7] ويسمح هذا التوصيل البطيء «للدوائر القصيرة» بالتشكيل، مما يحجب موجات النشاط الكهربائي في بعض المناطق بينما يسمح لها بالمرور في مناطق أخرى وهي ظاهرة تُعرف باسم تصادم الموجات الذي يسمح (عندما تكون الظروف مواتية) لموجات الكهرباء بأخذ منعطف على شكل حرف U خلال عضلة القلب، والسير في الاتجاه المعاكس قبل البدء في الدوران بسرعة حول نقطة ما، والتي يُشار إليها باسم إعادة الدخول، ومن ثم التسبب في اضطراب نظم القلب.[7] يجادل أولئك الذين يدعمون هذه النظرة (المعروفة باسم فرضية زوال الاستقطاب) أن تباطؤ التوصيل قد يفسر سبب ميل حدوث اضطراب نظم القلب المصاحب لبروغادا في منتصف العمر، حيث أن تفاقم العوامل الأخرى مثل التندب أو التليف المصاحب للكِبر يؤدي لاستثارة تباطؤ التوصيل الناجم عن الطفرة الوراثية. [20]
يشير آخرون إلى أن السبب الرئيسي لاضطراب نظم القلب هو الاختلاف في الخواص الكهربائية بين داخل القلب (الشغاف) وخارجه (التامور) (وهي فرضية تُعرف باسم إعادة الاستقطاب). [7] بمعنى أن شكل جهد الفعل يختلف بين شغاف القلب وغشاء التامور، حيث يُظهر جهد فعل خلايا عشاء التامور درجة ثُلمة بارزة بعد الارتفاع الأولي بسبب وجود تيار داخلي عابر، وهو أمر يكون أقل وضوحًا في خلايا الشغاف، ويظهر الفرق بين الشغاف والتامور بوضوح في البطين الأيمن. وبالنسبة لأولئك المصابين بمتلازمة بروغادا فإن هذه الاختلافات تزداد، مما يخلق فترة وجيزة في كل دورة قلبية يتدفق فيها التيار من الشغاف إلى التامور متسببا في ظهور نمط تخطيط القلب المميز، وتوصف الاختلافات في الخواص الكهربائية بين الشغاف والتامور على أنها «تشتت إعادة الاستقطاب عبر الجدار» والذي يمكن أن يؤدي إلى إحصار النبضات الكهربائية في بعض المناطق دون الأخرى في حالة إذا كان حجمه كبيرًا بما فيه الكفاية. مرة أخرى يمكن لهذا التصادم الموجي أن يسمح لموجات الكهرباء أن تنتقل في حركة دائرية يُعاد دخولها بدلا من انتقالها في اتجاه واحد، مما يسبب اضطراب نظم القلب. [7]
تُعتبر تغيرات بنية القلب أحد العوامل الأخرى التي تعزز اضطراب نظم القلب في متلازمة بروغادا.[20] ففي حين أن قلب المصابين بمتلازمة بروغادا قد يبدو طبيعيًا، إلا أن التندب أو التليف يظهر غالبًا في مناطق معينة من القلب، وبالتحديد في سبيل التدفق البطيني الأيمن. ونظرًا لأن متلازمة بروغادا يمكن أن تسببها طفرات في العديد من الجينات المختلفة، فمن الممكن أن تكون هناك آليات متنوعة هي المسؤولة عن اضطراب نظم القلب لدى المرضى المختلفين. [20]
التشخيص عدل
تخطيط كهربائية القلب عدل
تُشخص متلازمة بروغادا عن طريق تحديد أنماط مميزة أثناء إجراء تخطيط كهربية القلب. [12] ويتضمن هذا النمط وجود ارتفاع لقطعة إس تي في الأقطاب V 1 -V 3 مع ظهور إحصار فرع الحزمة الأيمن. وقد يكون هناك دليل على تباطؤ التوصيل الكهربائي في القلب، والذي يُستدل عليه بطول الفترة بي آر. قد تكون هذه الأنماط موجودة طوال الوقت، وقد لا تظهر إلا كاستجابة لأدوية معينة (انظر أدناه)، أو عندما يكون الشخص مصابًا بالحمى أو أثناء التمرين أو نتيجة لمحفزات أخرى. كما قد يصبح نمط تخطيط القلب أكثر وضوحًا وذلك بإجراء تخطيط القلب يتم فيه وضع بعض الأقطاب الكهربائية في مواقع مختلفة عن المعتاد.[21]
وُصفت ثلاثة أنماط لتخطيط القلب في متلازمة بروغادا [12]
- النمط الأول: ويحدث فيه ارتفاع مجوف الشكل للقطعة إس تي، ويصل ارتفاع النقطة جيه لـ 2 مم على الأقل (0.2 mV)، مع تنازل تدريج يتبعه موجة تي سلبية.
- النمط الثاني: نمط سرجي الشكل يكون فيه ارتفاع النقطة جيه 2 مم على الأقل وارتفاع القطعة إس تي 1 مم على الأقل يتبعها موجة تي موجبة أو ثنائية الطور. ويمكن رؤية هذا النمط في الأصحاء أحيانا.
- النمط الثالث: ويحتوي نمط مجوف (مثل النوع الأول) أو سرجي الشكل (مثل النوع الثاني)، مع ارتفاع للنقطة جيه أقل من 2 مم، وارتفاع للقطعة إس تي أقل من 1 مم. ويعتبر هذا النمط غير نادر في الأصحاء.
وفقًا للتوصيات الحالية فإنه لا يمكن تأكيد تشخيص متلامة بروغادا إلا بالاعتماد على النمط الأول فقط، وهو نمط يحدث إما تلقائيًا أو كاستجابةً للأدوية، ذلك لأن النمطين الآخرين يظهران في بشكل متكرر في الأشخاص الأصحاء. [8]
الاختبارات الاستفزازية عدل
يمكن لبعض الأدوية وخاصة مضادات اضطراب النظم التي تمنع تيار الصوديوم القلبي أن تكشف عن النمط الأول لتخطيط بروغادا في الأشخاص المعرضين للإصابة. وبالتالي يمكن استخدامها في المساعدة في إقامة التشخيص في المشتبه في إصابتهم بمتلازمة بروغادا (كأن يكون المشتبه به عانى من سكتة قلبية مجهولة السبب، أو كون أحد أفراد أسرته مصابا بمتلازمة بروغادا) دون أن يظهر لديهم النمط التشخيصي أثناء تخطيط كهربائية القلب. [2] فمثل هذه الحالات يمكن إعطائها أدوية حجب تيار الصوديوم في ظروف يمكن التحكم بها.[21] وتشمل الأدوية الأكثر شيوعا لهذا الغرض كل من أجمالين، فليكاينيد، وبروكاييناميد، مع اقتراحات تشير إلى أن الأجمالين قد يكون أكثر فعالية.[22] ويجب توخي الحذر عند إعطاء هذه الأدوية لوجود خطر التسبب في اضطراب نظم القلب. [21]
الاختبارات الجينية عدل
يمكن للاختبارات الجينية أن تكون مفيدة في تحديد المرضى المصابين بمتلازمة بروغادا، ويتم الاختبار بشكل أكثر شيوعا لأفراد عائلة الشخص الذ تم تشخيصه بمتلازمة بروغادا، أو في بعض الأحيان للمريض الذي يتوفى فجأة وبشكل غير متوقع.[5] ومع ذلك فإن تفسير نتائج الاختبارات الجينية يُمثل تحديا، فبعض أعضاء الأسرة التي يحمل كل أفرادها تباين وراثي محدد مصاحب لمتلازمة بروغادا قد تظهر عليهم أدلة الإصابة بالمتلازمة أثناء إجراء تخطيط كهربائية القلب، في حين لا يظهر ذلك على الأعضاء الآخرين.[5] وهذا يعني أن حمل الطفرة الجينية المرتبطة بمتلازمة بروغادا لا يعني بالضرورة أن يتأثر الشخص فعلا بالحالة، ولمزيد من التعقيد فالكثيرا من التغيرات التي تحدث في جين SCN5A لا تسبب أي مشاكل، وبالتالي ففي بعض الأحيان تُحدد المتغيرات الجينية في أشخاص لديهم متلازمة بروجادا لكنها لا تسبب المرض فعلا.[23]
فحوصات أخرى عدل
أحيانا تُستخدم دراسات الفيزيولوجيا الكهربية الاقتحامية لتقييم المخاطر على شخص لديه متلازمة بروغادا يعاني اضطراب نظم قلبي خطير،[24] وذلك عبر تمرير الأسلاك عبر الوريد لتنشيط وتسجيل الإشارات الكهربائية للقلب. كما يتم تنفيذ التقسيم الطبقي للمخاطر أحيانًا باستخدام جهاز تخطيط كهربائية القلب موسط الإشارة.[5] كما يُستخد أحيانًا جهاز تخطيط كهربائية القلب المحمول لتقييم ما إذا كان حدوث الدوخة أو الإغماء في شخص مصاب بمتلازمة بروجادا ناتج عن اضطراب نظم القلب أم سبب آخر مثل الإغماء الوعائي مهبمي.[25]
-
النمط الأول لمتلازمة بروغاد (لاحظ الوضع الغير قياسي للأقطاب، حيث وضع القطب V 5 مساحة وربي واحد فوق V 1 و V 6 يوضع مساحة intercostal واحد فوق V 2). .
-
النمط الثاني لمتلازمة بروغادا
إدراة الحالة عدل
يُعتبر الهدف الرئيسي أثناء علاج المصابين بمتلازمة بروغادا هو تقليل خطر الوفاة المفاجئة بسبب اضطرابات نظم القلب الخطيرة مثل الرجفان البطيني أو تسارع القلب البطيني المتعدد الأشكال.[26] وفي حين أن بعض المصابين يكونوا معرضون لمخاطر اضطرابات نظم القلب الخطيرة، إلا أن هذه المخاطر تقل في البعض الآخر، مما يعني أن النوع الأول قد يحتاج إلى علاج مكثف أكثر من غيرهم.[8] وبجانب علاج الشخص المصاب بمتلازمة بروغادا فإنه من المهم في كثير من الأحيان إجراء فحوصات لأفراد أسرهم المباشرين لتأكيد ما إذا كانوا مصابين هم أيضا. [8]
نمط الحياة عدل
يُمثل تقديم المشورة بشأن نمط الحياة خط العلاج الأول والمناسب لجميع المصابين بمتلازمة بروغادا بغض النظر عن مخاطر اضطرابات نظم القلب لديهم.[8] فيجب أن يُنصح المصابين بتمييز وتجنب الأشياء التي من شانها أن تزيد من مخاطر اضطرابات نظم القلب الخطيرة، ويشمل ذلك تجنب الإفراط في استهلاك الكحول، وتجنب بعض الأدوية، [12] وعلاج الحمى على الفور بالباراسيتامول.[8] وبالرغم من أن اضطرابات نظم القلب المُلاحظة في متلازمة بروغادا من المرجح أن تحدث بشكل عام أثناء الراحة أو حتى أثناء النوم، إلا أن بعض الأشخاص المصابين بالمتلازمة قد يعانون من اضطرابات نظم القلب أثناء ممارسة التمارين الرياضية الشاقة، لذلك قد ينصح بعض الأطباء المصابين بمتلازمة بروغادا بتجنب التمرينات الشاقة.[27] [28]
مزيل الرجفان القابل للزرع عدل
قد يوصى الأطباب بمقوم نظم القلب مزيل الرجفان القابل للزرع في المرضى الذين يكونون معرضون بشكل أكبر لموت القلب المفاجئ.[8] حيث تراقب هذه الأجهزة الصغيرة المزروعة تحت الجلد نظم القلب باستمرار، وإذا اكتشف المقوم اضطراب في نظم القلب يحتمل أن يكون مهددا للحياة، فإنه يمكن أن يوصل صدمة كهربائية صغيرة للقلب، والتي من شأنها أن تعيد الإيقاع الطبيعي للقلب.[29] كما يمكن أن يعمل هذا المقوم كناظمة قلبية اصطناعية تمنع البط الغير طبيعي لمعدل ضربات القلب والذي يمكن أن يحدث أيضًا للمصابين بمتلازمة بروغادا.
يُعتبر زرع مقوم نظم القلب مزيل الرجفان القابل للزرع إجراء منخفض المخاطر نسبيًا، وغالبًا ما يتم إجراؤه تحت التخدير الموضعي.[29] إلا أنه ومع ذلك يمكن أن تحدث بعض المضاعفات مثل العدوى والنزيف أو الصدمات غير الضرورية، والتي قد تكون خطيرة في بعض الأحيان.[30] ونظرًا لتكلفة المقوم وللمخاطر المرتبطة بزرعه فإنه لا يُنصح باستخدام هذه المقومات في جميع المصابين بالمتلازمة، وتُترك كخيار للأشخاص الذين يُعتبرون أكثر عرضة للوفاة القلبية المفاجئة. [8]
أدوية عدل
الكوينيدين هو دواء مضاد لاضطراب النظم قد يقلل فرص حدوث الإيقاعات المضطربة الخطيرة في بعض الأشخاص المصابين بمتلازمة بروغادا.[9] [31] ويُستخدم الكوينيدين بشكل متكرر في المصابين بالمتلازمة والذين لديهم مقوم نظم القلب مزيل الرجفان القابل للزرع وعانوا من نوبات اضطرابات نظم القلب المهددة للحياة، لكن قد يتم استخدامه أيضًا في المصابين المعرضين لمخاطر جسيمة لاضطرابات نظم القلب وليس لديهم مقوم نظم مناسب. [8]
كذلك يمكن استخدام دواء ايزوبرينالين (دواء يشبه الأدرينالين) في حالات الطوارئ للمصابين بالمتلازمة ويعانون من اضطراب نظم قلبي متكرر يُهدد حياتهم، والمعروف باسم «العاصفة الكهربائية». [8] ويجب إعطاء هذا الدواء بالتنقيط الوريدي وبالتالي فهو غير مناسب للاستخدام على المدى الطويل.
الاجتثاث بالقسطرة عدل
يُعتبر الاستئصال القسطري بالترددات الراديوية خيار علاجي إضافي للمصابين بمتلازمة بروجادا.[32] وفيه يتم تمرير أسلاك عبر وريد في الساق إلى القلب، أو من خلال ثقب صغير أسفل عظم القص. وتُستخدم هذه الأسلاك للعثور على المنطقة في القلب المسؤولة عن بدء اضطراب نظم القلب، حيث يُستخدم رأس أحد هذه الأسلاك لإحداث سلسلة حروق صغيرة، وإلحاق ضرر متعمد بالمنطقة التي تسبب المشكلة. وتشير التوصيات الحالية إلى أن هذا العلاج يجب أن يكون مخصصًا لمصابي متلازمة بروغادا الذين تعرضوا لصدمات متكررة من مقوم نظم القلب مزيل الرجفان القابل. [8]
علم الأوبئة عدل
يصاب بمتلازمة بروغادا من 1 إلى 30 في كل 10,000 شخص. [1] [2] وبالرغم من أن المصابين قد ولدوا بهذه الحالة، إلا أنه نادراً ما تظهر الأعراض في مرحلة الطفولة وعادة ما تظهر لأول مرة في مرحلة البلوغ، وفي حين أن الحالات النادرة التي ظهرت عليها الأعراض في مرحلة الطفولة تساوت فيها نسبة الذكور والإناث، إلا أن ظهور الأعراض في سن البلوغ كان أكثر في الذكور في كثير من الأحيان، وربما يرجع ذلك إلى ارتفاع مستويات هرمون التستوستيرون لدى الرجال. [2] [33]
التاريخ عدل
سُميت متلازمة بروغادا باسم أخصائيا القلب الإسبانيان بيدرو بروغادا وجوسيب بروغادا اللذين وصفا الحالة في عام 1992، [10] على الرغم من أن العلاقة بين نمط تخطيط القلب المميز والموت القلبي المفاجئ قد أٌبلغ عنها عام 1989.[34] ووُصفت متلازمة بروجادا كسبب لمتلازمة موت القلب المفاجئ غير المفسر والتي شوهدت في الرجال التايلانديين في عام 1997.[35] وقد حدد شقيقهم رامون بروغادا الطفرات الوراثية الأولى التي تؤثر على جين SCN5A المرتبط بالمتلازمة عام 1998، [36] ثم تعرف آخرون على العديد من الطفرات الأخرى التي تؤثر على ما لا يقل عن 19 جينًا. [13] أدت الدراسات التي أجريت في عام 2000 إلى نظريات متنافسة تحيط بالآليات التي يتم من خلالها توليد اضطرابات نظم القلب. [11] وتستمر الأبحاث حول متلازمة بروجادا، وتحديد المتغيرات الوراثية الجديدة، واستكشاف آليات عدم انتظام ضربات القلب، والبحث عن علاجات أفضل. [11]
انظر أيضًا عدل
مراجع عدل
- ^ أ ب ت ث ج ح خ "Brugada syndrome". Genetics Home Reference. مارس 2015. مؤرشف من الأصل في 2017-10-28. اطلع عليه بتاريخ 2017-10-28.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع غ "Brugada syndrome: A general cardiologist's perspective". European Journal of Internal Medicine. ج. 44: 19–27. أكتوبر 2017. DOI:10.1016/j.ejim.2017.06.019. PMID:28645806.
- ^ أ ب ت ث ج ح خ د "Brugada Syndrome". NORD (National Organization for Rare Disorders). 2016. مؤرشف من الأصل في 2017-02-11. اطلع عليه بتاريخ 2017-10-28.
- ^ أ ب "Brugada syndrome". Genetic and Rare Diseases Information Center (GARD) – an NCATS Program. 2017. مؤرشف من الأصل في 2017-10-17. اطلع عليه بتاريخ 2017-10-28.
- ^ أ ب ت ث ج ح خ "Brugada syndrome: clinical and genetic findings". Genetics in Medicine. ج. 18 ع. 1: 3–12. يناير 2016. DOI:10.1038/gim.2015.35. PMID:25905440.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض "Brugada Syndrome: Clinical, Genetic, Molecular, Cellular, and Ionic Aspects". Current Problems in Cardiology. ج. 41 ع. 1: 7–57. يناير 2016. DOI:10.1016/j.cpcardiol.2015.06.002. PMC:4737702. PMID:26671757.
- ^ أ ب ت ث ج ح خ د ذ "Brugada Syndrome: Cellular Mechanisms and Approaches to Therapy". Electrical diseases of the heart. Basic foundations and primary electrical diseases (ط. 2nd). London: Springer. ج. 1. 2013. ص. 497–536. ISBN:978-1-4471-4880-7. OCLC:841465583.
- ^ أ ب ت ث ج ح خ د ذ ر ز س "HRS/EHRA/APHRS expert consensus statement on the diagnosis and management of patients with inherited primary arrhythmia syndromes: document endorsed by HRS, EHRA, and APHRS in May 2013 and by ACCF, AHA, PACES, and AEPC in June 2013". Heart Rhythm. ج. 10 ع. 12: 1932–63. ديسمبر 2013. DOI:10.1016/j.hrthm.2013.05.014. PMID:24011539.
{{استشهاد بدورية محكمة}}: الوسيط|إظهار المؤلفين=6غير صالح (مساعدة) - ^ أ ب "Efficacy of quinidine in high-risk patients with Brugada syndrome". Circulation. ج. 110 ع. 13: 1731–7. سبتمبر 2004. DOI:10.1161/01.CIR.0000143159.30585.90. PMID:15381640.
- ^ أ ب "Right bundle branch block, persistent ST segment elevation and sudden cardiac death: a distinct clinical and electrocardiographic syndrome. A multicenter report". Journal of the American College of Cardiology. ج. 20 ع. 6: 1391–6. نوفمبر 1992. DOI:10.1016/0735-1097(92)90253-J. PMID:1309182.
- ^ أ ب ت "Brugada syndrome: More than 20 years of scientific excitement". Journal of Cardiology. ج. 67 ع. 3: 215–20. مارس 2016. DOI:10.1016/j.jjcc.2015.08.009. PMID:26627541.
- ^ أ ب ت ث "Drugs and Brugada syndrome patients: review of the literature, recommendations, and an up-to-date website (www.brugadadrugs.org)". Heart Rhythm. ج. 6 ع. 9: 1335–41. سبتمبر 2009. DOI:10.1016/j.hrthm.2009.07.002. PMC:2779019. PMID:19716089.
- ^ أ ب "An international compendium of mutations in the SCN5A-encoded cardiac sodium channel in patients referred for Brugada syndrome genetic testing". Heart Rhythm. ج. 7 ع. 1: 33–46. يناير 2010. DOI:10.1016/j.hrthm.2009.09.069. PMC:2822446. PMID:20129283.
{{استشهاد بدورية محكمة}}: الوسيط|إظهار المؤلفين=6غير صالح (مساعدة) - ^ "The genetic basis of Brugada syndrome: a mutation update". Human Mutation. ج. 30 ع. 9: 1256–66. سبتمبر 2009. DOI:10.1002/humu.21066. PMID:19606473.
- ^ "Genetic basis of Brugada syndrome". Heart Rhythm. ج. 4 ع. 6: 756–7. يونيو 2007. DOI:10.1016/j.hrthm.2007.03.015. PMC:1989771. PMID:17556198.
- ^ أ ب ت ث ج ح "Ion Channel Disorders and Sudden Cardiac Death". International Journal of Molecular Sciences. ج. 19 ع. 3: 692. فبراير 2018. DOI:10.3390/ijms19030692. PMC:5877553. PMID:29495624.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Diagnostic dilemmas: overlapping features of brugada syndrome and arrhythmogenic right ventricular cardiomyopathy". Frontiers in Physiology. ج. 3: 144. 2012. DOI:10.3389/fphys.2012.00144. PMC:3358709. PMID:22654761.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "High prevalence of concealed Brugada syndrome in patients with atrioventricular nodal reentrant tachycardia". Heart Rhythm. ج. 12 ع. 7: 1584–94. يوليو 2015. DOI:10.1016/j.hrthm.2015.03.015. PMID:25998140.
- ^ "Sinus node disease in subjects with type 1 ECG pattern of Brugada syndrome". Journal of Cardiology. ج. 61 ع. 3: 227–31. مارس 2013. DOI:10.1016/j.jjcc.2012.12.006. PMID:23403368.
- ^ أ ب ت ث "The pathophysiological mechanism underlying Brugada syndrome: depolarization versus repolarization". Journal of Molecular and Cellular Cardiology. ج. 49 ع. 4: 543–53. أكتوبر 2010. DOI:10.1016/j.yjmcc.2010.07.012. PMC:2932806. PMID:20659475.
- ^ أ ب ت "How to perform and interpret provocative testing for the diagnosis of Brugada syndrome, long-QT syndrome, and catecholaminergic polymorphic ventricular tachycardia". Circulation: Arrhythmia and Electrophysiology. ج. 4 ع. 6: 958–64. ديسمبر 2011. DOI:10.1161/CIRCEP.111.965947. PMID:22203660.
- ^ "Intravenous drug challenge using flecainide and ajmaline in patients with Brugada syndrome". Heart Rhythm. ج. 2 ع. 3: 254–60. مارس 2005. DOI:10.1016/j.hrthm.2004.11.025. PMC:1474213. PMID:15851314.
- ^ "Genetic testing in heritable cardiac arrhythmia syndromes: differentiating pathogenic mutations from background genetic noise". Current Opinion in Cardiology. ج. 28 ع. 1: 63–71. يناير 2013. DOI:10.1097/HCO.0b013e32835b0a41. PMC:3705648. PMID:23128497.
- ^ "Programmed Ventricular Stimulation for Risk Stratification in the Brugada Syndrome: A Pooled Analysis". Circulation. ج. 133 ع. 7: 622–30. فبراير 2016. DOI:10.1161/CIRCULATIONAHA.115.017885. PMC:4758872. PMID:26797467.
{{استشهاد بدورية محكمة}}: الوسيط|إظهار المؤلفين=6غير صالح (مساعدة) - ^ "Use of implantable loop recorders in patients with Brugada syndrome and suspected risk of ventricular arrhythmia". Europace. ج. 14 ع. 6: 898–902. يونيو 2012. DOI:10.1093/europace/eur319. PMID:21979995.
- ^ "The Brugada Syndrome: A Rare Arrhythmia Disorder with Complex Inheritance". Frontiers in Cardiovascular Medicine. ج. 3: 9. 2016. DOI:10.3389/fcvm.2016.00009. PMC:4842929. PMID:27200363.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Brugada Syndrome and Exercise Practice: Current Knowledge, Shortcomings and Open Questions". International Journal of Sports Medicine. ج. 38 ع. 8: 573–581. يوليو 2017. DOI:10.1055/s-0043-107240. PMID:28625016.
- ^ "Brugada syndrome, exercise, and exercise testing". Clinical Cardiology. ج. 38 ع. 5: 323–6. مايو 2015. DOI:10.1002/clc.22386. PMID:25955277.
- ^ أ ب "Advances in implantable cardioverter defibrillator therapy". Expert Review of Cardiovascular Therapy. ج. 14 ع. 3: 291–9. 2016. DOI:10.1586/14779072.2016.1131124. PMID:26653411.
- ^ "Implantable cardioverter-defibrillator harm in young patients with inherited arrhythmia syndromes: A systematic review and meta-analysis of inappropriate shocks and complications". Heart Rhythm. ج. 13 ع. 2: 443–54. فبراير 2016. DOI:10.1016/j.hrthm.2015.09.010. PMID:26385533.
- ^ "Quinidine revisited". The American Journal of Medicine. ج. 122 ع. 4: 317–21. أبريل 2009. DOI:10.1016/j.amjmed.2008.11.019. PMID:19249010.
- ^ "Catheter ablation to prevent sudden cardiac death". International Journal of Cardiology. ج. 237: 29–33. يونيو 2017. DOI:10.1016/j.ijcard.2017.03.135. PMID:28433554.
- ^ "Brugada syndrome in children – Stepping into unchartered territory". Annals of Pediatric Cardiology. ج. 10 ع. 3: 248–258. سبتمبر 2017. DOI:10.4103/apc.APC_49_17. PMC:5594936. PMID:28928611.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Ventricular fibrillation without apparent heart disease: description of six cases". American Heart Journal. ج. 118 ع. 6: 1203–9. ديسمبر 1989. DOI:10.1016/0002-8703(89)90011-2. PMID:2589161.
- ^ "Arrhythmogenic marker for the sudden unexplained death syndrome in Thai men". Circulation. ج. 96 ع. 8: 2595–600. أكتوبر 1997. DOI:10.1161/01.CIR.96.8.2595. PMID:9355899.
- ^ "Genetic basis and molecular mechanism for idiopathic ventricular fibrillation". Nature. ج. 392 ع. 6673: 293–6. مارس 1998. Bibcode:1998Natur.392..293C. DOI:10.1038/32675. PMID:9521325.
| في كومنز صور وملفات عن: متلازمة بروغادا |