ثلاثي فلوريد البروم
مركب كيميائي
ثلاثي فلوريد البروم هو مركب كيميائي بين هالوجيني صيغته BrF3، ويوجد على شكل سائل أصفر شاحب اللون.
| ثلاثي فلوريد البروم | |
|---|---|
| المعرفات | |
| CAS | 7787-71-5 |
| بوب كيم | 24594 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | BrF3 |
| الكتلة المولية | 136.90 غ/مول |
| المظهر | سائل أصفر شاحب |
| الكثافة | 2.84 غ/سم3 |
| نقطة الانصهار | 8.77 °س |
| نقطة الغليان | 126 °س |
| الذوبانية في الماء | يتفاعل |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
التحضير عدل
يحضر المركب من تفاعل البروم مع الفلور؛[2] وفق التفاعل التالي:
وكان بول لوبو قد تمكن سنة 1906 من تحضيره عند الدرجة 20 °س.[3]
يمكن أن يستحصل أيضاً على ثلاثي فلوريد البروم من حدوث تفاعل عدم تناسب لمركب أحادي فلوريد البروم:[4]
الخواص عدل
يوجد المركب في الشروط القياسية على شكل سائل أصفر شاحب، بلون بشبه لون القش،[4] وهو قابل للاسترطاب، ويتفاعل بشكل عنيف من الماء.
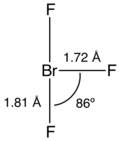
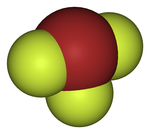
للمركب بنية جزيئية على شكل T، ويبلغ طول الرابطة المحورية 1.81 أنغستروم، أما الرابطة الاستوائية فيبلغ طولها 1.72 أنغستروم؛ أما زاوية الرابطة بين المستويين فتبلغ 86.2 °.[5][6]
الاستخدامات عدل
يعد ثلاثي فلوريد البروم من العوامل المفلورة الجيدة، ويستخدم من أجل تحضير سداسي فلوريد اليورانيوم.[7]
طالع أيضاً عدل
المراجع عدل
- ^ أ ب ت BROMINE TRIFLUORIDE (بالإنجليزية), QID:Q278487
- ^ Georg Brauer (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 169.
- ^ Lebeau P. (1906). "The effect of fluorine on chloride and on bromine". Annales de Chimie et de Physique. ج. 9: 241–263.
- ^ أ ب Simons JH (1950). "Bromine(III) Fluoride (Bromine Trifluoride)". Bromine (III) Fluoride - Bromine Trifluoride. Inorganic Syntheses. ج. 3. ص. 184–186. DOI:10.1002/9780470132340.ch48. ISBN:978-0-470-13234-0.
- ^ Gutmann V (1950). "Die Chemie in Bromitrifluorid". Angewandte Chemie. ج. 62 ع. 13–14: 312–315. DOI:10.1002/ange.19500621305.
- ^ Meinert H (1967). "Interhalogenverbindungen". Zeitschrift für Chemie. ج. 7 ع. 2: 41–57. DOI:10.1002/zfch.19670070202.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (بالإنجليزية) (2 ed.). Butterworth-Heinemann. ISBN:0-08-037941-9.
| ثلاثي فلوريد البروم في المشاريع الشقيقة: | |
| |