تناضح
التناضح أو الخاصية الأسموزية أو الحلول أو التنافذ أو الأزموزية أو التنافذ الغشائي أو الأسموزية أو الانتضاح[1] أو الانتشار الغشائي (باليونانية: ὠσμός «دفع») (بالإنجليزية: Osmosis)، هي صافي حركة انتقال جزيئات الماء عبر غشاء نصف نافذ من منطقة ذات نسبة ذوائب منخفضة (مثل ماء عذب) إلى منطقة ذات كثافة ذوائب مرتفعة (تركيز أعلى للذوائب، أي ماء بحر مالح مثلا) دون الحاجة لاستهلاك طاقة. الغشاء النصف نافذ يسمح بنفوذ الماء (المذيب) ولا يسمح بنفوذ الذوائب (solute) مما يؤدي إلى تدرج في الضغط عبر الغشاء.
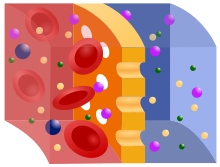


الخاصية الأسموزية شائعة في الطبيعة ولها شأن كبير في الكائنات الحية، وعلى الأخص في تنظيم المحتوى المائي في الخلايا الحية والأنسجة.
كما تستخدم الخاصية الأسموزية وقدرة الأغشية على الفصل بين محاليل مركزة ومحاليل مخففة، وتجد تطبيقات في الطب وفي تقنية الأنظمة وكذلك في إنتاج الطاقة الكهربية معتمدا على الخاصية الأسموزية.
كذلك توجد تقنية فصل الماء العذب من ماء البحر، وهي تعتمد على الأسموزية المعكوسة. إذا اردنا استخلاص ماء عذب من ماء مالح فيجب تشديد الضغط على ناحية الماء المالح فتعبر منه جزيئات ماء عبر الغشاء النصف نافذ إلى ناحية الماء العذب، ولا تعبر الأملاح. أي نحتاج في تلك الحالة إلى بذل طاقة للتغلب على الخاصية الأسموزية لتسير بالعكس.
نأتي بأنبوب زجاجي ذو فرعين على شكل U ونفصل بين فرعيه بوضع غشاء نصف نافذ. ونملأ الفرع اليميني بالماء ونملأ الفرع اليساري بمحلول ماء مذاب فيه ملح، بحيث يكون ارتفاع عمود الماء في الفرع الأيمن مساويا لارتفاع المحلول الملحي في الفرع اليساري وننتظر بعضاً من الوقت. نشاهد بعد فترة من الزمن أن عمود الماء في الفرع الأيمن ينخفض، ويرتفع عمود المحلول في الفرع اليساري المحتوي على الملح. ويظل الماء في الفرع الأيمن خاليا من الملح، ويبقى الملح محصورا في عموده في المحلول الملحي.
ويظل الماء ينتقل عبر الغشاء من عامود الماء النقي إلى عامود المحلول الملحي حتي يصل إلى نهاية عظمى عند ارتفاع ثابت. ويسمى فرق ارتفاع عمودي الماء والمحلول بالضغط الإسموزي أو ضغط التناضح.
أمثلة على عملية التناضح عدل
عملية التناضح عملية حيوية وموجودة في العديد من العمليات الطبيعية ومنها:
- انتقال الماء من وإلى الخلايا الحية مثل خلايا النباتات والهيموغلوبين وخلايا بشرية أخرى وغيرها.
- يستغل التناضح في التقنية لفصل المواد، وطبيا في الغسيل الكلوي (تنقية دم المريض من البول عند مرضى الكلى المصابين بقصور كبير في عمل الكلى).
تفسير أساسي عدل
يقع التناضح عند وجود غشاء شبه نافذ. عند إغراق خلية في كأس من الماء جزيئات الماء تمرّ من الوسط المنخفض التركيز (hypotonic) خارج الخلية إلى الوسط مرتفع التركيز (hypertonic) في الخلية عبر الغشاء شبه النافذ لتحقيق حالة توازن للضغط (isotonic). الغشاء نافذ بطريقة انتقائية فهو يسمح فقط بمرور مواد معينه ويمنع مرور مواد غيرها
تفسير مرور الماء عبر الغشاء النصف نافذ من الماء إلى محلول ملحي: تتصرف حبيبات الملح الذائبة في الماء كما لو كانت غازا، ويكون لها ضغط معين يعتمد على تركيز المحلول. هذا الضغط يحاول أن يزيد من حجمه وذلك بالضغط على سطح المحلول في الأنبوب من أسفل إلى أعلى. فيرتفع سطح المحلول ساحبا معه ماء من الناحية الأخرى للغشاء (الغشاء يسمح بمرور جزيئات الماء ولا يسمح بمرور جزيئات الملح). يرتفع عمود المحلول تحت هذا الضغط الداخلي فيه (ضغط جزيئات الملح) وينخفض عمود الماء في ناحية الماء النقي.
أمثلة من التناضح عدل
الضغط التناضحي أو الضغط الإسموزي هو السبب الرئيسي لامتصاص النباتات للماء، فماء التربة بصفة عامة يكون ضغطه التناضحي أقل من الضغط الموجود داخل الشعيرات الماصة في الجذور مما يؤدي إلى مرور الماء من التربة إلى الجذور وليس العكس. عندما توضع خلية من نبتة في محلول مرتفع التركيز تبدأ هذه النبتة في الانكماش بسبب خروج الماء منها وانتشاره في المحلول مرتفع التركيز لتكوين حالة توازن للضغط.
يمكن مشاهدة التناضح كذلك عند وضع شرائح البطاطا في محلول من الماء المالح، فبعد مدة تبدأ هذه الشرائح في فقدان الماء والانكماش. كما نشاهد في مزارع الكرز انفجار ثمرات الكرز عند هطول مطر لمدة طويلة حيث تمتص الثمرة - بما فيها من محلول سكري - ماء زائدا عن الحد ويتمزق غلافها.
تحلية المياه عدل
يُستخدم أسلوب اسمه «الضغط الإسموزي العكسي» لتحلية مياه البحر ومياه الآبار واستخراج ماء عذب منها. تلك العملية تتم بطريقة معكوسة لظاهرة الضغط الإسموزي المعروفة طبيعيا. في تلك الطريقة يوضع الماء المالح تحت ضغط عال، أعلى من الضغط الإسموزي، فتنتقل جزيئات الماء من الماء المالح إلى الماء العذب عبر الغشاء، ونحصل على ماء عذب. تعتمد تلك الطريقة على مقدار الضغط المسلط على المحلول وعلى نوع الغشاء. وتوجد أبحاث كثيرة بغرض الوصول إلى التركيبة المثلى للغشاء بالطرق الكيميائية للارتفاع بكفاءة عملية الفصل.
تطبيق قانون الغازات عدل
تنطبق قوانين الغازات للغازات المثالية مثل قانون بويل وقانون جاي-لوساك وقانون أفوجادرو أيضا على حالة سائل مخفف.
فيكون الضغط الإسموزي:
- متناسبا طرديا مع التركيز المولي للمادة المذابة.
- متناسبا طرديا مع درجة الحرارة المطلقة.
- في المحاليل يعتمد الضغط الإسموزي على عدد جسيمات المادة المذابة فقط (تركيزها المولي).
- يبلغ الضغط الإسموزي لمحلول مكون من 1 مول من المذاب في 4و22 لتر سائل مذيب 101,325 كيلوباسكال (1 ضغط جوي قياسي) عند درجة حرارة 273 كلفن (0 درجة مئوية).
تؤدي تلك الشروط إلى قانون فان هوف للضغط الإسموزي: «الضغط الإسموزي يعادل ضغط غاز له نفس العدد من الجسيمات n عند درجة حرارة T»، فيكون:
تعني في هذه المعادلة الضغط الإسموزي بوحدة باسكال.
- c = n/V التركيز المولي في المحلول.
- k ثابت بولتزمان.
- R ثابت الغازات العام.
- T درجة الحرارة المطلقة كلفن.
ينطبق هذا القانون في صورته الحالية على سائل مخفف (<0,1 مول /لتر) حيث أن قوانين الغازات تنطبق في حالة الضغوط المنخفضة (حيث يكون التآثر بين الجسيمات بعضها البعض مهملا).
الصيغة الثرموديناميكية عدل
تجري الظاهرة الأسموزية من تلقاء نفسها فهي عملية «خلط» - تنفصل مادة من طورها وتختلط في مادة أخرى مكونة طور جديد. وتسبب عملية تجري من تلقاء نفسها في نظام مغلق إلى خفض الإنثالبي الحر (طاقة غيبس الحرة) وارتفاع في أنتروبية النظام. وفي حالة الظاهرة الأسموزية تعمل الخاصية المميزة للغشاء النصف نافذ على منع تساوي التركيز على ناحيتي الغشاء عند الوصول إلى التوازن الترموديناميكي - فيوجد لدينا طورين للمادة منفصلان عن بعضهما في جميع الأزمنة. (في الواقع يمكن القول بأن النظام يتكون من ثلاثة أطوار، إذا أخذنا الغشاء أيضا في الاعتبار).
فيكون التغير في الإنثالبي الحر الكلي في الخلية الأسموزية مساويا لمجموع التغيرين للإنثالبي في طوري النظام:
حيث الأرقام (1) و (2) مميزة للمحلولين في الخلية الأسموزية على ناحيتي الغشاء النصف نفاذ. وعندما يكون الغشاء نافذا لأحد المواد (مثل مادة سائل المذيب)، فيمكن وصف العلاقة بين الإنثالبي الحر G وكمية المادة بالعلاقتين:
حيث:
- كمية المادة مول التي تعبر الغشاء.
ونظرا لكون الكمية المكتسبة في الطور (2) يعادل الكمية المفقودة من الطور (1) فينتج للتغير الكلي في الإنثالبي الحر:
وبالتالي:
وطالما لم يصل النظام إلى حالة التوازن الترموديناميكي ( )، فينطبق بالنسبة إلى الكمونات الكيميائية:
وعند الوصول إلى حالة التوازن ( ):
هذا بالنسبة إلى مادة واحدة مذابة في سائل. أما إذا كان لدينا عدة مواد ذائبة في السائل فلابد من صياغة العلاقات المذكورة أعلاه بأخذ الكمونات الكيميائية لجميع المواد المذابة في الاعتبار (أنظر قسم الجهد الأسموزي في المحاليل الغير مثالية).
شرط الوصول إلى حالة التوازن في الظاهرة الأسموزية يعتمد على أن تكون الكمونات الكيميائية للمادة التي تعبر الغشاء (وهي تكون في الغالب السائل المذيب) تكون كموناتها على الناحيتين متساوية. وطالما كان في النظام اختلاف في الكمونين فسوف تنتقل جسيمات للمادة في اتجاه الكمون المنخفض.
الضغط الأسموزي للمحاليل غير المثالية عدل
لا ينطبق قانون فان هوف عل المحاليل غير المثالية (المحاليل المركزة) حيث يحدث فيها تآثر بين الجزيئات بعضها البعض ولا يمكن إهمالها. عندئذ لا بد من استخدام الكمون الكيميائي من معادلة جيبس العامة. في حالة التوازن الترموديناميكي يبلغ الإنثالبي الحر (طاقة غيبس الحرة) في الخلية الأزموزية نهاية صغرى:
وبافتراض أن العملية تتم في درجة حرارة ثابتة، تتبسط المعادلة إلى:
وعندما يكون الضغط المحيط متساويا يبلغ التغير في الضغط الأزموزي:
أي أن الضغط الأزموزي ينتج من التركيزات المولية الناشئة عن تغير جميع الكمونات الكيميائية . وقد أخدت في هذه المعادلة تأثيرات الخلط في الاعتبار. وفي أغلب الأحوال نهمل تلك التأثيرات التي تحدث بين المواد الذائبة بعضها البعض وكذلك تركيز السائل المذيب:
كما يمكننا تبسيط المعادلة مرة ثانية بإهمال التآثر بين الجزيئات الذائبة وجزيئات السائل المذيب أيضا. في تلك الحالة يمكن اعتبار الفاعلية الكيميائية لتلك المواد مساوية 1، ونصل إلى معادلة تقريبية:
ولكن يجب ملاحظة أن هذا التقريب يؤدي عند التركيزات العالية إلى أخطاء قد تصل إلى 50 %، خصوصا بسبب إهمالنا للتآثرات بين الجزيئات بعضها البعض.
يُسمى الضغط الأزموزي السالب الإشارة أحيانا «الجهد الأزموزي» ويرمز له بالرمز .
الضغط الأسموزي في الكائنات الحية عدل
للضغط الأسموزي أهمية كبيرة في تكوين الكائنات الحية وسير العمليات الحيوية فيها. فكل خلية محاطة بغشاء يكون حائلا بالنسبة إلى الانتقال العشوائي للمواد، إلا الماء الذي هو السائل المذيب فيمكنه الانتقال عبر الغشاء. وحتى الخلية نفسها فيوجد في داخلها جسيمات تغطيها أغشية هي الأخرى تسمح بمرور أنواع الجزيئات. وتوجد النباتات في حالة تبادل مستمر مع الماء، حيث تمتص وتنقل وتطرد ماء. وخلايا الحيوانات الفقرية تحيطها سائل الدم والبلازما.
تطبيقات عدل
قياس الأسمولية عدل
يعتبر قياس الأسمولية (بالإنجليزية: Osmolarity) بواسطة الطرق الأسموزية من أحد الأعمال الرئيسية في مجال العلوم البيولوجية. ويستخدم في حالة العمل على خلايا حية محلول منظم لتفادي حدوث تفاعلات غير مرغوبة فيها تحت تأثير الإجهاد الأسموزي. فمثلا عند فصل البروتوبلاست (جبلة مجردة) يمكن أن يتسبب استخدام محلول منظم زائد التركيز في تمزيق. وعند تركيب تلك المحاليل المنظمة في المختبر فيمكن قياس المولية الأسموزية لها ومقارنتها بالقيم المناسبة لها.
في الطب عند العلاج بالقسطرة الوريدية يستخدم محلول ملحي بغرض عدم الإضرار بخلايا الجسم عن طريق الضغط الأسموزي. وهو محلول مكون من الماء ويحتوي على 0,9 % (وزنا) من ملح الطعام، وتبلغ المولية الأسموزية لهاذا المحلول 330 mosmol/لتر وهي تعادل تقريبا تلك لبلازما الدم، وهو يعادل ضغطا أسموزيا قدره 7و0 ميجا باسكال. أما في حالة استخدام ماء نقيا عند العلاج بالقسطرة الوريدية فقد يؤدي ذلك الفرق في الضغط في انفجار بعض خلايا الدم.
غسيل الكلى عدل
تستخدم أغشية في عملية غسيل الكلى لها خاصية السماح لجزيئات وأيونات يبلغ حجمها أقل من حجم معين، وفي نفس الوقت تكون مانعة لمرور جزيئات بروتين أو أحماض نوكليين. بتلك الطريقة يمكن فصل مواد ذات تركيب جزيئي صغير الحجم وعزلها أو خفض كمياتها إلى مستويات مناسبة. يُملأ - بحسب الطريقة المستخدمة - المحلول الديالي في وعاء (خرطوم ديالي) ويغطس هذا في محلول ديالي ويبقى فيه فترة زمنية. أو يبقى المحلول المراد دياليته، مثلما في حالة ديال الدم، معزولا بواسطة غشاء عن محلول التنقية. وتطبق طرق الديال في الطب بغرض تنظيف الدم، كما تُستغل في الصناعة وفي هندسة العمليات الصناعية (مثل تحضير البيرة الخالية من الكحول).
تناضح عكسي عدل
يتم التناضح العكسي أو «الضغط الأسموزي المعكوس» عن طريق رفع الضغط في نظام مكون من ماء ومحلول به مادة ذائبة ويفصلهما غشاء نصف نافذ. يعمل رفع الضغط فوق ناحية ماء المحلول على زيادة تركيز المحلول (يعمل رفع الضغط على المحلول على إجبار جزيئات الماء المرور عبر الغشاء في الاتجاه المعاكس، أي من المحلول إلى الماء العذب). وتستخدم تلك الطريقة في فصل الماء العذب عن ماء البحر المالحة. ولكن لابد من بذل طاقة لتوليد هذا الضغط.
(في عملية استخلاص ماء عذب من ماء البحر يتم عادة عن طريق تبخير مياه البحر وتكثيف البخار. أي يتم هذا عن طريق إمداد ماء البحر الموجود في غلاية بطاقة حرارية من الخارج لإجراء التبخير. ويعطينا الضغط الأسموزي المعكوس طريقة ثانية لاستخلاص ماء عذب من ماء البحر (اقرأ محطة تناضح عكسي). أي تتفق الطريقتان في كونهما تحتاجان إلى طاقة خارجية لفصل الملح عن الماء، وهذا ما تقوله قوانين الترموديناميكا.
محطة قوى بالضغط الأسموزي عدل
بنيت فكرة محطة القوى التي تعمل بالضغط الأسموزي علي استغلال الشغل الناتج من الضغط الأسموزي لإنتاج الطاقة. وتستغل محطة القوى الفرق في الكمون الكيميائي بين ماء البحر المحتوي على الملح والكمون الكيميائي للماء العذب، وتشغيل عنفة يحرك مولد كهربائي لإنتاج التيار الكهربائي.
يمر ماء عذب في أنبوب عبارة عن غشاء نصف نافذ خلال ماء البحر فيرتفع الضغط في الماء المالح. ويوجه جزء من الماء ذو الضغط العالي (وهو ماء نصف مالح حيث اكتسب جزءا من الماء العذب)، يوجه إلى عنفة لإدارته، بينما الجزء الأكبر من هذا الماء (2/3 الكمية) إلى مبادل للضغط يعمل على رفع ضغط ماء البحر المسحوب.[2]
وقد أنشئت محطات قوى تجريبية للعمل بهذه الطريقة بغرض دراستها وتحسينها، ولكن لم تدخل حيز التطبيق الصناعي لإنتاج الطاقة. تصل قدرة المحطات التجريبية إلى نحو 3 ميجاوات وتعمل منذ عدة سنوات ويجرى تطويرها وتحسينها.[3] وقد شيدت أول محطة طاقة صغيرة في النرويج في خليج أوسلو في نوفمبر 2009 وتسمى محطة توليد الطاقة بـ«ستاتكرافت» (بالنرويجية: Statkraft Hurum saltkraftverk) وهي حاليًا أكبر محطة تستغل ضغط التناضح لإنتاج الكهرباء.[4]
انظر أيضاً عدل
المراجع عدل
- ^ منير البعلبكي؛ رمزي البعلبكي (2008). المورد الحديث: قاموس إنكليزي عربي (بالعربية والإنجليزية) (ط. 1). بيروت: دار العلم للملايين. ص. 396. ISBN:978-9953-63-541-5. OCLC:405515532. OL:50197876M. QID:Q112315598.
- ^ Statkraft: Osmotic Power (PDF, engl.) نسخة محفوظة 16 مايو 2017 على موقع واي باك مشين.
- ^ Bericht der Financial Times Deutschland vom 23. Jan. 2008 نسخة محفوظة 26 مايو 2020 على موقع واي باك مشين.
- ^ Statkraft Pressemitteilung 24. Nov. 2009 (engl.) نسخة محفوظة 29 أبريل 2012 على موقع واي باك مشين.
| تناضح في المشاريع الشقيقة: | |
| |